(8分)I、通过火法冶金炼出的铜是粗铜,含杂质金、银、铁、锌等金属和少量矿物杂质(与酸不反应)。制作电器及其他仪器产品时必须要求是纯铜,为此以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯。
表:几种物质形成沉淀时的pH
| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀时的pH | 7.6 | 2.7 | 5.7 | 4.7 |
| 完全沉淀时的pH | 9.7 | 3.7 | 8.5 | 7.3 |
(2)在精炼铜的过程中,Cu2+浓度逐渐降低,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。甲同学设计了如下除杂流程:

|
②操作①是 ,根据上表数据分析,除杂方案中能够除去的杂质金属阳离子是
(填化学式)。
II、重金属离子对河流海洋等会造成严重的污染。某化工厂产生的废水(pH=2.0,密度为1g·mL-1)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01mol·L-1,排放前拟用沉淀法回收这两种金属,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
a、NaOH b、Na2S c、KI d、Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=
某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(提示:Ag2sO4微溶于水):
第一步:向溶液中滴加过量的 溶液(填化学式),其目的是检验CO32-。并将其除去;发生反应的离子方程式为 。
第二步:加入过量的 溶液(填化学式),其目的是 ;
第三步:过滤,再向滤液中加入 溶液(填化学式),发生反应的离子方程式 。
(8分)为了达到下表所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入对应的空格中。
| 实验要求 | 化学试剂 |
| 1.检验酒精中是否有水 | |
| 2.区别CH4和C2H4两种无色气体 | |
| 3.验证味精是否有食盐 | |
| 4.除去Fe2O3中的Al2O3 | |
A.酸性高锰酸钾B.硝酸银溶液和硝酸C.氢氧化钠溶液D.无水硫酸铜粉末
(4分)现提供如下除杂试剂和提纯方法:
| 除杂试剂 | ① 酸性高锰酸钾溶液 ②溴水 ③饱和碳酸钠溶液 ④氢氧化钠溶液 |
| 提纯方法 | A蒸馏 B萃取 C分液 D洗气 |
| 甲 | 除杂试剂 | 提纯方法 |
| 甲烷(乙烯) | | |
| 乙酸乙酯(乙酸) | | |
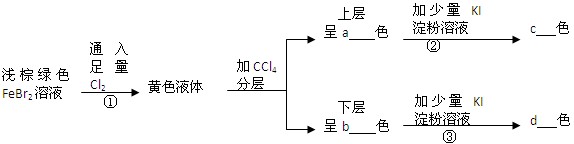
(12分)海带中含有丰富的碘。为了从海中提取碘,某研究性学习小组设计并进行了以下实验:
请填写下列空白:
⑴步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
| A.烧杯 | B.坩埚 | C.表面皿 | D.泥三角 E、酒精灯 F、干燥器 |
⑶步骤④反应的离子方程式是 。
⑷步骤⑤中,某学生选择用苯来提取碘的理由是 。
⑸请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法: 。
(1)(7分)现有以下有机物:(用序号回答下列各问)
① 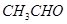 ②
② 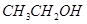 ③
③  ④
④ 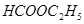
①能与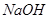 溶液反应的有_________________;
溶液反应的有_________________;
②能与银氨溶液反应产生银镜的是____________________;
③既能发生消去反应,又能发生酯化反应的有___________________;
④核磁共振氢谱图中有3个吸收峰,面积比为3:2:1的是___________;
(2).(8分)为进行Ⅰ项中的除杂实验(括号内为杂质),请从Ⅱ项中选出一种试剂,从Ⅲ项中选出一合适的实验操作方法分离,将标号填在后面的答案栏内。
| Ⅰ 除杂实验 | Ⅱ 试剂 | Ⅲ 操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯酚) | A.饱和Na2CO3溶液 B.NaCl晶体 C.NaOH溶液 D.CaO | a.蒸馏 b.分液 c.盐析、过滤 d.萃取 | ① | | |
| ②乙醇(水) | ② | | | ||
| ③肥皂(甘油、水) | ③ | | | ||
| ④乙酸乙酯(乙酸) | ④ | | | ||
b. 向a中所得的银氨溶液中滴入少量葡萄糖溶液,混合均匀后,放在水浴中加热3min~5min,即可在试管内壁上形成银镜,则此反应的化学方程式为③(葡萄糖的结构简式用G-CHO表示):