下列各组物质的分离或提纯,应选用下述方法的哪一种?(用编号填空)
| A.分液 | B.过滤 | C.萃取 | D.蒸馏 E、蒸发结晶 F、加热分解 |
③ 用自来水制取蒸馏水 ;④ 除去KCl固体中少量的KClO3固体 ;
⑤ 分离植物油和水 ; ⑥ 除去水中的沙土 ;
(12分)已知:I2+2S2O===S4O+2I-。相关物质的溶度积常数见下表:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是 (用化学方程式表示)。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是 。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用 作滴定指示剂,滴定终点的现象是 。
②CuCl2溶液与KI反应的离子方程式为 。
③该试样中CuCl2·2H2O的质量百分数为 。
(8分)在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题: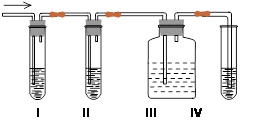
(1)I、II、III、IV装置可盛放的试剂是I ;II ;III ;IV (填序号)。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.酸性KMnO4溶液 |
(3)使用装置II的目的是 。
(4)使用装置III的目的是 。
(5)确定含有乙烯的现象是 。
(10分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
| A.萃取分液法 | B.加热分解 | C.结晶法 | D.分液法 |
(1)___________分离饱和食盐水和沙子的混合物;
(2)___________从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(3)___________分离水和煤油的混合物;
(4)___________分离水和酒精;
(5)___________分离溴水中的溴和水。
(10分)硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。 已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。
已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。
请回答:(1)写出A与氢氧化钠溶液反应的化学方程式: 。
(2)上述流程中试剂②应该是 (填以下字母编号)。
| A.氢氧化钠 | B.氧化铝 | C.氨水 | D.水 |
。
(4)计算溶液F中c(Mg2+)= ( 25℃时,氢氧化镁的Ksp=5.6×10-12)。
(5)工业生产中将固体C灼烧后的产物与KNO3、KOH固体加热共熔制备净水剂K2FeO4,同时获得一种亚硝酸盐,请写出制得K2FeO4的化学方程式: 。
(4分)物质分离提纯常用方法有:
| A.萃取 | B.分液 | C.过滤 | D.结晶 |
请为下列各组混合物的分离或提纯选择最佳方法(选填标号)
(1)提纯含少量NaCl杂质的KNO3 (2)除去Fe(OH)3胶体中的少量KCl
(3)分离柴油和水的混合物 (4)用工业酒精制取无水乙醇