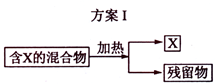
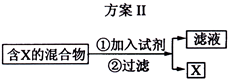
环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮: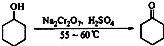
环己醇、环己酮和水的部分物理性质见下表:
| 物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)★ | 0.9624 | 能溶于水 |
| 环己酮 | 155.6(95)★ | 0.9478 | 微溶于水 |
| 水 | 100.0 | 0.9982 | |
(1)酸性Na2Cr2O7溶液氧化环己醇反应的△H<0,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧杯中,在55~60℃进行反应。
反应完成后,加入适量水,蒸馏,收集95~100℃的馏分,得到主要含环己酮和水的混合物。
①酸性Na2Cr2O7溶液的加料方式为 。
②蒸馏不能分离环己酮和水的原因是 。
(2)环己酮的提纯需要经过以下一系列的操作:
a. 蒸馏,收集151~156℃的馏分; b. 过滤;
c. 在收集到的馏分中加NaCl 固体至饱和,静置,分液;
d. 加入无水MgSO4固体,除去有机物中的少量水。
①上述操作的正确顺序是 (填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需 。
③在上述操作c中,加入NaCl 固体的作用是 。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有 种不同化学环境的氢原子。
下列实验现象和结论相符的是
| | 操作及现象 | 结论 |
| A | 某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 溶液中一定含有CO32- |
| B | 某溶液中加入硝酸银,产生白色沉淀 | 溶液中一定含有Cl- |
| C | 用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 | 溶液中有Na+,无K+ |
| D | 向某溶液中先加几滴KSCN溶液,无明显现象,再滴氯水,溶液变红 | 溶液中一定含有Fe2+ |
只用一种试剂,区别下列四种溶液Na2SO4、Al2(SO4)3、FeCl2、(NH4)2SO4,此试剂是
| A.稀盐酸 | B.BaCl2溶液 | C.AgNO3溶液 | D.NaOH浓溶液 |
下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
②除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤,分液、干燥、蒸馏;
③除去CO2中少量的SO2:气体通过盛饱和碳酸氢钠溶液的洗气瓶;
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
| A.①② | B.②④ | C.③④ | D.②③ |
只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3、FeCl3和CuSO4六种溶液,,这种试剂是
| A.Ba(OH)2 | B.H2SO4 | C.NaOH | D.AgNO3 |
分离下列混合物,应选用蒸馏操作的是
| A.汽油和柴油 | B.溴水 |
| C.硝酸钾和氯化钠的混合物 | D.四氯化碳和水 |
下列各组溶液中,不用任何其他试剂就能鉴别的是( )
| A.Na2SO4 H2SO4 AlCl3 BaCl2 | B.HCl NaOH K2SO4 NaHCO3 |
| C.AlCl3 KHCO3 NaCl Na2SO4 | D.NaOH FeCl3 MgCl2 K2SO4 |
对于某些离子的检验及结论一定正确的是( )
| A.通入Cl2后,溶液变为黄色,加淀粉液后溶液变蓝,则原溶液中一定有I- |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定有SO42- |
| C.加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |