不能用一种试剂鉴别的一组物质是 ( )
| A.苯、乙二醇、四氯化碳 | B.苯酚溶液、2,4-己二烯、甲苯 |
| C.己烷、3--己烯、甲苯 | D.苯酚溶液、硫氰酸钾溶液、氢氧化钠溶液 |
可以用分液漏斗分离的一组混合物是
| A.酒精和碘 | B.苯和水 | C.乙酸和水 | D.溴和四氯化碳 |
某学生设计了如下图所示的方法对A盐溶液进行鉴定: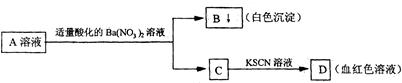
由此分析,下列结论中不正确的是 ( )
| A.A中一定有Fe3+ | B.C中一定有Fe3+ |
| C.A可能为Fe2(SO4)3 | D.B一定为BaSO4 |
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释不正确的是( )
| A.某溶液中加入稀硫酸再加入铜粉,共热,铜粉溶解且有红棕色气体产生,说明原溶液中含有NO3- |
| B.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,有有色产物生成且能溶于浓硝酸 |
| C.某溶液中加入NaOH溶液,加热能产生使湿润的红色石蕊试纸变蓝的气体,说明原溶液中含有NH4+ |
| D.在KI淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应 |
乙烯中混有SO2气体,欲除去SO2,得到较纯净的乙烯,最好依次通过下列哪组试剂的洗气瓶
| A.酸性KMnO4溶液、浓H2SO4 | B.溴水、浓H2SO4 |
| C.浓H2SO4、酸性KMnO4溶液 | D.NaOH溶液、浓H2SO4 |
现有一瓶签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验: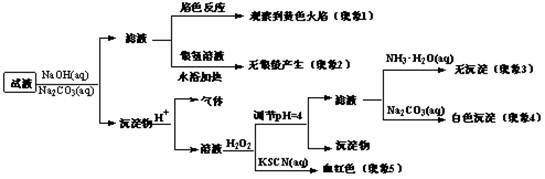
已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。
该同学得出的结论正确的是
| A.根据现象1可推出该试液中含有Na+ |
| B.根据现象2可推出该试液中并不含有葡萄糖酸根 |
| C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+ |
| D.根据现象5可推出该试液中一定含有Fe2+ |
下列实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 目的 | 分离方法 | 原理 |
| A. | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B. | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C. | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
| D. | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
下列操作不能达到目的的是
| 选项 | 目的 | 操作 |
| A. | 配制100 mL 1.0 mol/L CuSO4溶液 | 将25 g CuSO4·5H2O溶于100 mL蒸馏水中 |
| B. | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C. | 在溶液中将MnO4-完全转化为Mn2+ | 向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 |
| D. | 确定NaCl溶液中是否混有Na2CO3 | 取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
用图所示装置检验乙烯时不需要除杂的是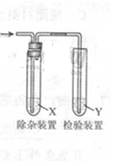
| | 乙烯的制备 | 试剂X | 试剂Y |
| A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
| B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
| C | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
| D | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | Br2的CCl4溶液 |
下列依据相关实验得出的结论正确的是( )
| A.向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| C.将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯 |
| D.向某溶液中滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |