下列实验操作中,错误的是
| A.蒸发操作时,不能使混合物中的水分完全蒸干后,才停止加热 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
把95g含有某一种氯化物杂质的氯化镁粉末溶于水后,与足量AgNO3溶液反应,生成300g AgCl沉淀,则该氯化镁中的杂质可能是
| A.NaCl | B.A1C13 | C.KCl | D.CaCl2 |
要除去NaCl溶液中含有的Ca2+、Mg2+、SO42-、HCO3-等离子,通常采用以下四种试剂:①Na2CO3②BaCl2③NaOH④HCl。加入试剂合理的操作顺序是
| A.①②③④ | B.③①②④ | C.④②①③ | D.③②①④ |
有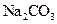 、
、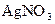 、
、 、
、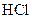 、
、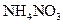 五种无标签溶液,为鉴别它们,取四只试管分别装入一种溶液,向上述四只试管中加入少许剩下的一种溶液X,下列结论错误的是( )
五种无标签溶液,为鉴别它们,取四只试管分别装入一种溶液,向上述四只试管中加入少许剩下的一种溶液X,下列结论错误的是( )
A.若只有三只试管出现沉淀时,则X溶液是 溶液 溶液 |
B.若四支试管中都没有明显现象时,则X溶液是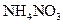 溶液 溶液 |
C.若只有一只试管出现气体,两只试管出现沉淀时,则X溶液是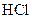 溶液 溶液 |
D.若只有两只试管出现沉淀时,则X溶液是 溶液 溶液 |
下列叙述不正确的是( )
A.向澄清石灰水中通入CO2产生白色沉淀 ,再通入过量CO2,沉淀消失 ,再通入过量CO2,沉淀消失 |
B.向AlCl3溶液中滴加NaOH溶液,产生白色沉淀,再加入过量NaOH溶液,沉淀消失 |
| C.向AgNO3溶液中滴加氨水,产生白色沉淀,再加入过量氨水,沉淀消失 |
| D.向Na2SiO3溶液中滴加盐酸,产生白色沉淀,再加入过量盐酸,沉淀消失 |
有AgNO3、HCl、KSCN、NaOH四种溶液,只用一种试剂鉴别,这种试剂是( )
| A.FeCl2溶液 | B.Na2CO3溶液 | C.氯水 | D.FeCl3溶液 |
某无色溶液中可能含有Na+、Fe2+、Br-、CO32-、I-、SO32-六种离子中的几种。①在该溶液中滴加足量氯水后,有气泡产生、溶液呈橙黄色;②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;③向淀粉溶液中滴加橙黄色溶液未变蓝色。根据上述实验事实推断,在该溶液中肯定存在的离子组是 ( )
| A.Na+、Br-、CO32- | B.Na+、 I-、SO32- |
| C.Fe2+、I-、SO32- | D.Fe2+、Br-、CO32- |
化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是( )
| A.定性检验SO42—,将BaCl2溶液用HNO3酸化 |
| B.为了提高KMnO4溶液的氧化能力,用盐酸将其酸化 |
| C.配制FeCl3溶液时通常加少量HNO3酸化,减小其水解程度 |
| D.检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液 |
为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是
| | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴化钠溶液(NaI) | 氯水、CCl4 | 萃取、分液 |
| B | CO(CO2) | 饱和NaHCO3溶液 | 洗气 |
| C | FeSO4(Fe2(SO4)3) | 足量铁屑 | 过滤 |
| D | CO2(SO2) | NaOH | 洗气 |
下列物质的提纯方法可能属于化学变化的是( )
| A.蒸馏 | B.过滤 | C.分液 | D.洗气 |