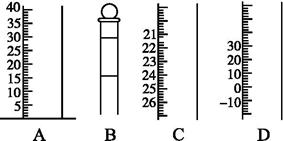
硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得。已知:Na2S2O3在酸性溶液中不能稳定存在;硫代硫酸钠与碘反应的离子方程式为:2S2O32-+I2→S4O62-+2I- 。
(Ⅰ)制备Na2S2O3·5H2O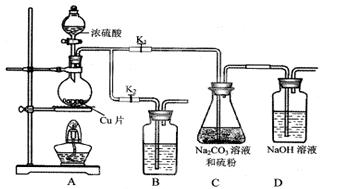
打开K1,关闭K2,向放有铜片的圆底烧瓶中加入足量浓硫酸,加热。圆底烧瓶中发生反应的化学方程式是 。
C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少。C中碳酸钠的作用
是 。“停止C中的反应”的操作是 。
过滤C中的混合液。将滤液加热浓缩、冷却结晶、过滤、洗涤、烘干,得到产品。“过滤”用到的玻璃仪器是(填仪器名称) 。
装置B中盛放的试剂是(填化学式) 溶液,其作用是 。
(Ⅱ)用I2的标准溶液测定产品的纯度
取5.5g产品,配制成100mL溶液。取10.00mL溶液,以淀粉溶液为指示剂,用浓度为0.050mol/L I2的标准溶液进行滴定,相关数据记录如下表所示。
| 编号 | 1 | 2 | 3 |
| 溶液的体积/mL | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.95 | 17.10 | 20.05 |
Na2S2O3·5H2O在产品中的质量分数是 (用百分数表示,且保留1位小数)。
(1)图甲是实验室常用的一种仪器,其名称是____ ;其主要用途是________;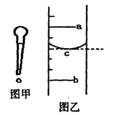
(2)小明用某规格的量筒量取一定体积的液体,液面位置如图乙,则其量得液体体积为______________(用a、b来表示)
(3)下图是某研究性小组设计的一个储气装置图。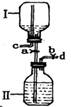
①将气体存于Ⅱ瓶中,下列说法不正确的是 。
| A.打开止水夹a,b,将气体从导管d通入,可将气体储存在Ⅱ瓶中 |
| B.作为储气或取气时都无需在C处安装止水夹 |
| C.该装置主要缺陷是C导管上未装止水夹 |
| D.该装置也可用作制取氢气的发生装置 |
下列与实验相关的叙述正确的是 。
A.要除去溴苯中的少量液溴,可先加入适量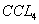 莘取,然后再分液 莘取,然后再分液 |
| B.溶液的浓度越高,或者蒸发的速度越快,析出的晶体就越细小 |
| C.减压过滤完毕时,应先关闭水龙头,再拆连接抽气泵和吸滤瓶的橡胶管,以防倒吸 |
| D.电解精炼铜过程中阳极产生的阳极泥为粗铜中含有的锌、金、银等杂质 |
下列有关实验操作或判断正确的是______。
| A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大 |
| B.用干燥的蓝色石蕊试纸检验氯气 |
| C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 |
| D.实验室制取NO气体时,既可用排水法收集又可用排空气法收集 |
F.观察钾元素焰色反应的操作:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察
G.NH3能使湿润的红色石蕊试纸变蓝色
下列实验操作或叙述正确的是 (填序号,多选倒扣分,扣完为止。)
| A.乙醇中含有少量水可加入金属钠再蒸馏制得无水乙醇 |
| B.将无水乙醇和浓硫酸按体积比3:1混合,加热至140°C制取乙烯 |
| C.蔗糖水解用稀硫酸作催化剂,加热一段时间,然后加入银氨溶液检验是否发生了水解 |
| D.在鸡蛋白溶液中加入浓HNO3,微热后会生成黄色物质 |
F.植物油和裂化汽油可用溴水鉴别
 ,其毒性较大。某研究性学习小组为了变
,其毒性较大。某研究性学习小组为了变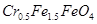 (
( 的化合价依次为+3、+2),设计了如下实验流程:
的化合价依次为+3、+2),设计了如下实验流程: