氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等。为获得纯净的氧化铜,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
⑵ 步骤Ⅱ的目的是除硫酸亚铁。操作步骤是先滴加H2O2溶液,稍加热,当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以调整溶液pH在一定范围之内,加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1。
①写出用H2O2溶液除去硫酸亚铁的离子方程式____________________________。
②调整pH 的范围应该在____________之间。
⑶ 步骤Ⅲ的目的是得到CuSO4·5H2O晶体。操作是将溶液加热蒸发至有晶膜出现时,停止加热,_____________,水浴加热烘干。采用水浴加热的原因是____ 。
⑷ 该同学用CuSO4溶液进行如下探究实验:取A、B两支试管,分别加入 2 mL 5%H2O2溶液,再向H2O2溶液中分别滴入0.1 mol·L-1 FeCl3和CuSO4溶液各1 mL,摇匀,观察到滴入FeCl3 溶液的试管产生气泡更快,由此得到结论:Fe3+对H2O2溶液分解的催化效率比Cu2+高,该同学的结论是否正确________(填正确或错误),请说明原因 。
(5)16克硫酸铜固体投入水中形成1升溶液,则该溶液显 性(填“酸性”或“碱性”或“中性”),溶液中所有阳离子总数 0.1NA(填“等于”或“大于”或“小于”),若在上述新配制溶液加入稀硫酸再加入铁片产生氢气速率会明显加快,原因是 ;室温下、若在上述新配制溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时c(Cu2+)=________________mol·L-1(Kap[Cu(OH)2]=2.2×10-20)。
下列实验操作可以达到实验目的的是 。
| A.只用溴的四氯化碳溶液就能鉴别乙烷与乙烯 |
| B.将蔗糖溶于水,加热后再加入少量新制的Cu(OH)2就可检验蔗糖的水解产物 |
| C.用玻棒取少许油脂的皂化反应液,滴于装有热水的试管中,振荡,若无油滴浮在液面上,说明油脂皂化完全。 |
| D.溴在有机溶剂中的溶解度比在水中的溶解度大,因此可用乙醇萃取溴水中的溴 |
下列实验操作或叙述正确的是 (填序号,多选倒扣分,扣完为止。)
| A.乙醇中含有少量水可加入金属钠再蒸馏制得无水乙醇 |
| B.将无水乙醇和浓硫酸按体积比3:1混合,加热至140°C制取乙烯 |
| C.蔗糖水解用稀硫酸作催化剂,加热一段时间,然后加入银氨溶液检验是否发生了水解 |
| D.在鸡蛋白溶液中加入浓HNO3,微热后会生成黄色物质 |
F.植物油和裂化汽油可用溴水鉴别
(12分)(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图3—2所示的游码尺上画出游码的位置(画“|”表示)。
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 | | | | | |
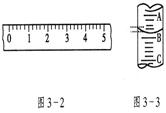
(2)图3—3表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量筒中的液体的体积是__________mL。
(3)用18mol?L—1的硫酸溶液配制0.5mol?L—1的硫酸溶液250mL所需的玻璃仪器为___________。
(4分)下列有关实验操作或判断不正确的是______。
| A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大 |
| B.用干燥的pH试纸测定氯水的pH |
| C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 |
| D.实验室制取NO气体时,既可用排水法收集又可用排空气法收集 |
F.观察钾元素焰色反应的操作:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,透过蓝色钴玻璃进行观察
G.制备氢氧化亚铁时,将盛有NaOH溶液的滴管,伸入硫酸亚铁溶液中