配制一定物质的量浓度的某溶液,下列情况会使配制结果偏低的是( )
| A.未冷却即转移、定容 | B.未洗烧杯及玻璃棒 |
| C.定容时俯视刻度线观察液面 | D.容量瓶中原有少量蒸馏水 |
在实验室利用浓盐酸和MnO2制氯气,制备装置中应安装分液漏斗而不是长颈漏斗,有关理由叙述错误的是
| A.尽量避免HCl挥发到空气中 | B.长颈漏斗不便于添加液体 |
| C.防止氯气扩散到空气中造成污染 | D.便于控制加入盐酸的量 |
关于下列各实验装置的叙述中,不正确的是( )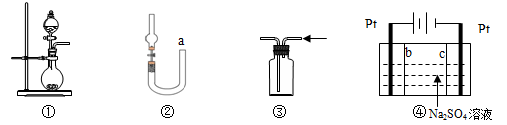
| A.装置①可用于实验室制取少量NH3或O2 |
| B.可用从a处加水的方法检验装置②的气密性 |
| C.实验室可用装置③收集H2、NH3 |
| D.利用装置④制硫酸和氢氧化钠,其中b为阳离子交换膜、c为阴离子交换膜 |
下列实验合理的是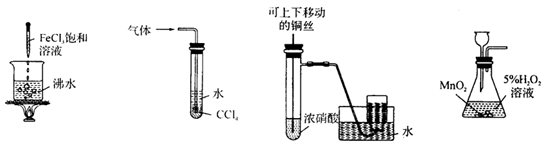
① ② ③ ④
| A.①实验只能得到红褐色沉淀 | B.②实验吸收氨气,并防止倒吸 |
| C.③实验制备并收集少量NO2气体 | D.④实验制备并收集少量O2气体 |
下列实验不能达到目的的是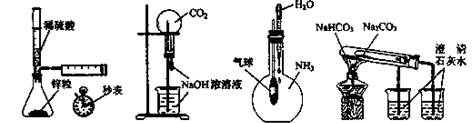
A B C D
| A.测定一定时间内生成H2的反应速率 | B.用CO2的做喷泉实验 |
| C.验证NH3易溶于水 | D.比较Na2CO3和NaHCO3的热稳定性 |
下列有关实验用品的使用或操作的叙述中,正确的是( )
| A.用红色石蕊试纸检验溶液的酸性 |
| B.称量NaOH固体时,将NaOH直接放在托盘中的纸片上 |
| C.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 |
| D.容量瓶用于配制一定体积、一定浓度的溶液,不能作为反应容器使用 |
下列实验操作中,所用仪器合理的是( )
| A.用托盘天平称取25.20gNaCl |
| B.用四氯化碳萃取碘的饱和水溶液中的碘分液时,水从分液漏斗下口流出,碘的四氯化碳溶液从漏斗上口倒出. |
| C.在蒸发皿中放入NaCl溶液,加热、蒸发制取NaCl晶体 |
| D.用100mL容量瓶配制50mL0.1mol/L的盐酸 |
关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是
| A.①②③④ | B.②③ | C.①②④ | D.②③④ |
下列配制1.0mol/L的NaOH溶液的操作不会造成误差的是
| A.称量后转移固体时不小心把少量固体洒到烧杯外 |
| B.干净的容量瓶又用蒸馏水洗涤了一遍 |
| C.转移过程中不小心把几滴溶液滴在外面 |
| D.加水定容时,加水过多,倒出后并恢复到刻度线水平 |
