在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后
| A.整个溶液变紫色 | B.整个溶液变为棕黄色 |
| C.上层为无色,下层为紫红色 | D.下层无色,上层紫红色 |
用98%的浓H2SO4(密度为1.84 g/mL)配制1 mol·L-1的稀H2SO4 100mL,配制过程中可能用到下列仪器:
①100mL量筒;②10mL量筒;③50mL烧杯;④托盘天平;⑤100mL容量瓶;⑥胶头滴管;⑦玻璃棒。按使用出现的先后顺序排列正确的是
| A.②⑥③⑦⑤ | B.④③⑤⑦⑥ | C.①③⑦⑤⑥ | D.②⑤⑦⑥ |
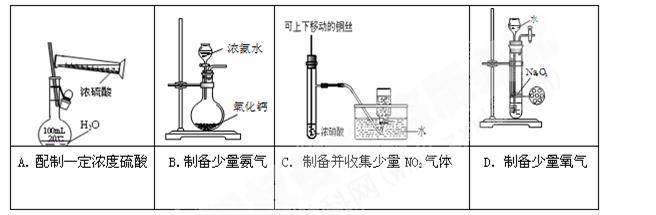
具备基本的化学实验技能是进行科学探究的基础和保证。下列有关实验操作正确的是 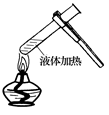
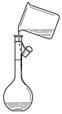
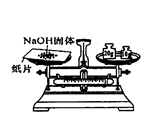
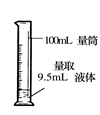
| A.给液体加热 | B.转移溶液 | C.称取NaOH固体 | D.量取液体 |
下列图示对应的实验操作均正确的是( )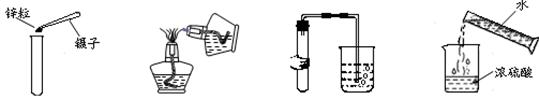
| A.向试管中加锌粒 | B.点燃另一酒精灯 | C.检查装置的气密性 | D.稀释浓 硫酸 硫酸 |
下列实验过程能引起结果偏高的是
①配制100gl0%CuSO4溶液,称取l0g硫酸铜晶体溶于90g水中
②测定硫酸铜晶体中结晶水的百分含量时,所用的晶体已经受潮
③配制一定物质的量浓度的硫酸溶液时,定容时俯视容量瓶的刻度线
④质量分数为10%和90%的两种硫酸等质量混合配制50%的硫酸溶液
| A.①④ | B.②④ | C.②③ | D.②③④ |
现有一种简单可行的测定阿伏加德罗常数的方法,具体步骤为:(1)将固体NaCl细粒干燥后,准确称出m克NaCl固体并转移到定容仪器a中。(2)用滴定管b向a仪器中滴加某液体 c,不断振荡,加至a仪器的刻度线,计算出NaCl固体的体积为Vcm3,再通过NaCl的体积和质量,即可算出阿伏加德罗常数.上述操作中的abc分别指
c,不断振荡,加至a仪器的刻度线,计算出NaCl固体的体积为Vcm3,再通过NaCl的体积和质量,即可算出阿伏加德罗常数.上述操作中的abc分别指
| A.量筒、酸式滴定管、水 | B.容量瓶、碱式滴定管、苯 |
| C.量筒、碱式滴定管、水 | D.容量瓶、酸式滴定管、四氯化碳 |
下列实验操作中错误的是 
| A.蒸发结晶时应将溶液蒸干 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| D.称量时,应该遵循“左物右码”的原则 |
每做一次焰色反应实验,都要用一种试剂洗净铂丝,这种试剂是
| A.稀盐酸 | B.NaOH溶液 | C.稀硫酸 | D.Na2CO3溶液 |
关于萃取的下列说法中不正确的是( )
| A.该实验使用的主要仪器是分液漏斗 |
| B.用酒精萃取溴水中的溴单质的操作可选用分液漏斗 |
| C.碘的四氯化碳溶液呈紫红色 |
| D.萃取、分液前需对分液漏斗检漏 |