用下列方法测定空气中的污染物含量:将一定体积的空气通入吸收剂,并测定其电导的变化(导体的电阻愈小,它的电导愈大),如测定H2S的含量,若用CuSO4溶液吸收,可测定很大浓度范围内的H2S,但电导变化不大;若用浓溴水吸收,仅限于低浓度范围内的H2S,但有很高的灵敏度。现要兼顾吸收容量与灵敏度,测定空气中Cl2的含量,则应选用下列吸收剂中的
| A.Na2SO3溶液 | B.KI溶液 |
| C.NaOH溶液 | D.H2O |
用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞作为指示剂,造成测定结果偏高的原因可能是
| A.配制标准溶液的NaOH中混有Na2CO3杂质 |
| B.滴定终点读数时,俯视滴定管的刻度,其他操作正确 |
| C.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗 |
| D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液 |
下面是一段关于酸碱中和实验操作的叙述:①取一锥形瓶,用待测NaOH溶液润洗两次。②在一锥形瓶中加入25 mL待测NaOH溶液。③加入几滴石蕊试剂做指示剂。④取一支酸式滴定管,洗涤干净。⑤直接往酸式滴定管中注入标准酸溶液,进行滴定。⑥左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶。⑦两眼注视着滴定管内盐酸溶液液面下降,直至滴定终点。文中所述操作有错误的序号为
| A.④⑥⑦ | B.①⑤⑥⑦? | C.③⑤⑦ | D.①③⑤⑦ |
中和相同体积、相同pH的H2SO4、HCl、CH3COOH三种溶液,所用相同浓度的NaOH的体积分别是V1、V2、V3,则三者的关系是:
| A.V1=V2=V3 | B.V1>V2>V3 | C.V3>V1>V2 | D.V1=V2<V3 |
用已知浓度的盐酸滴定由NaOH固体配成的溶液时,下列操作会使滴定结果偏低的是
| A.NaOH固体称量时间过长 | B.盛放标准盐酸的滴定管用碱液润洗 |
| C.用酚酞作指示剂 | D.固体NaOH中含有Na2O杂质 |
量筒和滴定管所盛放液体的凹面,都在10 mL刻度,若都采用仰视读数,则前者比后者的读数
| A.大于 | B.小于 | C.等于 | D.不能比较 |
用标准盐酸滴定未知浓度NaOH溶液时,若测定结果偏高,产生误差的原因可能是
A.滴定时,装NaOH溶 液的锥形瓶未用NaOH溶液润 液的锥形瓶未用NaOH溶液润 洗 洗 |
| B.酸式滴定管用蒸馏水洗后,用标准盐酸润洗 |
| C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失 |
| D.滴定前仰视读取了酸式滴定管的读数,滴定后读数正确 |
咖喱是一种烹饪辅料,若沾到白色衬衣上,用普通肥皂洗涤时,黄色污渍变成红色,经水漂洗后红色又恢复到黄色,据此现象,你认为咖喱汁与下列何种试剂有相似的化学作用
| A.品红溶液 | B.石蕊试液 | C.氯水 | D.KI淀粉溶液 |
关于下列各装置图的叙述中,不正确的是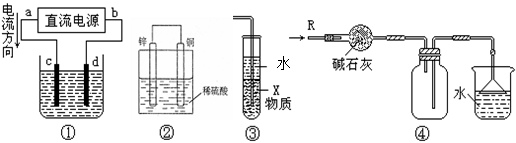
| A.若采用装置①精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液。 |
| B.装置②是原电池,能将化学能转化为电能,锌电极发生氧化反应 |
| C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
| D.装置④可用于干燥、收集氨气,并吸收多余的氨气 |
