在中和滴定实验中,下列操作不影响测定结果的是( )
| A.滴定管用蒸馏水洗净后,直接装滴定液 |
| B.锥形瓶用蒸馏水洗净后,再用待测液润洗 |
| C.滴定过程中,锥形瓶里的液体溅到瓶外 |
| D.用蒸馏水冲洗附在锥形瓶内壁上的液滴 |
在常温时,将V1 mL C1 mol/L CH3COOH溶液中滴加到V2 mL C2 mol/L NaOH溶液中,下列结论中,错误的是
| A.如果V1=V2,C1=C2,则混合溶液中c (CH3COO-) =" c" (Na+) |
| B.如果混合溶液的pH=7,则混合溶液中c (CH3COO-) =" c" (Na+) |
| C.如果混合溶液的pH>7,则可能V1C1 = V2C2 |
| D.如果V1=V2,且混合溶液的pH<7,则C1>C2 |
下列实验中,①配制—定物质的量浓度的溶液②pH试纸的使用③过滤④蒸发⑤溶解,均用到的仪器是
| A.烧杯 | B.漏斗 | C.玻璃棒 | D.胶头滴管 |
化学是一门以实验为基础的学科,掌握基本实验方法和操作技能是做好化学实验的基础。下列有关化学实验基本知识的描述不正确的是
| A.丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B.过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C.验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl- |
| D.检验某溶液中是否含有SO42-的方法是先向该溶液中加入BaCl2溶液,再加入稀HNO3 |
某学生欲用已知物质的量浓度的HCl测定未知浓度的NaOH溶液,将HCl置于滴定管,氢氧化钠溶液置于锥形瓶,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定未知浓度的NaOH溶液,滴定到终点时锥形瓶中颜色变化为 。
(2)下列操作中可能无法会怎样影响所测NaOH溶液浓度(填偏大.偏小或不影响)
A.酸式滴定管未用标准浓度的HCl润洗就直接注入标准盐酸
B.读数时,开始平视,结束时俯视 液面
液面
(3)某学生根据3次实验记录有关数据如下:
| 滴定次数 | 待测NaOH溶液体积(mL) | 0.1000mol/L HCl溶液的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
请选择合理的数据计算NaOH溶液的物质的量浓度:c(NaOH)=________________。
下列关于实验原理、操作的叙述,不正确的是 ( )
| A.排水法收集的CO2要比排空气法收集的CO2纯度高,所以我们首选排水法收集 |
| B.配制溶液时,俯视刻度线来定容,会使得所配溶液浓度偏高 |
| C.纸层析实验中,滤纸上的试样点可以用毛细管来点,使试样点的面积小 |
| D.除去乙酸乙酯中的乙酸,可以用饱和的碳酸钠溶液 |
实验室保存下列试剂,有错误的是
| A.浓盐酸易挥发,盛在无色密封的玻璃瓶中 |
| B.碘易升华,保存在盛有水的棕色试剂瓶中 |
| C.液溴易挥发,盛放在用水密封的用玻璃塞塞紧的棕色试剂瓶中 |
| D.溴化银保存在棕色瓶中 |
下列实验现象描述正确的是
| A.红热的铜丝在氯气中燃烧,产生棕色的烟 |
| B.碘水中加入少量汽油振荡静置后,下层液体为紫色 |
| C.往溴水中加入碘化钠溶液充分反应后,溶液为无色 |
| D.向FeCl2溶液中滴入KSCN溶液,溶液变为血红色 |
下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 氟化氢的沸点高于氯化氢 | HF分子间存在氢键,而HCl分子间几乎不存在氢键 |
| B | 将SO2气体通入氯水中,氯水褪色 | SO2具有漂白性 |
| C | MgCl2溶液中加入浓氨水,出现白色沉淀 | 碱性:NH3·H2O > Mg(OH)2 |
| D | 用pH试纸测得CH3COONH4溶液的pH=7 | CH3COONH4不能水解 |
下列物质与常用危险化学品的类别不对应的是
A.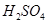 、 、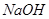 ——腐蚀品 ——腐蚀品 |
| B.CH4、CH3CH2OH(酒精)——易燃液体 |
| C.K、 Na——遇湿易燃物品 |
D.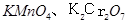 —— 氧化剂 —— 氧化剂 |