某铁的氧化物粉末可能含有FeO、Fe2O3中的一种或两种.一化学兴趣小组同学利用以下装置测定铁的氧化物的组成,请协助完成,并回答有关问题.
(1)李同学利用1mol/L的硫酸、KSCN溶液、酸性高锰酸钾溶液,确定其组成.
| 编号 | 实验操作 | 实验现象与结论 |
| ① | 取少量粉末放入试管中,注入1mol/L的硫酸 | 粉末逐渐溶解,溶液呈黄绿色 |
| ② | 将“①”中所得溶液分成两份;向其中一份滴加几滴KSCN溶液,振荡 | 若溶液变为______,说明有Fe2O3存在 |
| ③ | 在另一份中加入少量KMnO4溶液 | 若溶液______,说明有FeO存在 |
 CO↑+CO2↑+H2O,并拟用下列装置进行定量探究.
CO↑+CO2↑+H2O,并拟用下列装置进行定量探究.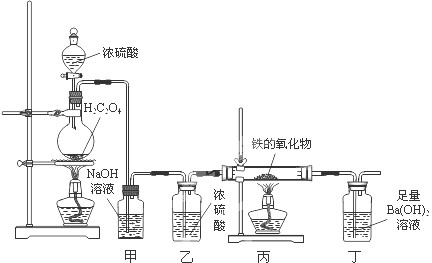
①装置甲的作用是______;装置丁中的实验现象是______.
②实验开始时,王同学发现打开分液漏斗旋塞,浓硫酸无法滴下,原因是______.
③若丙中铁的氧化物质量为3.04g,完全反应后丁中生成沉淀的质量为9.85g.试通过计算确定该铁的氧化物的成分及其物质的量之比.
 分馏石油
分馏石油

