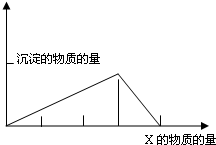
 将物质X逐渐加入(或滴入)Y溶液中,其生成沉淀的量与加入X的物质的量关系如下图所示,符合图示情况的是
将物质X逐渐加入(或滴入)Y溶液中,其生成沉淀的量与加入X的物质的量关系如下图所示,符合图示情况的是
| A | B | C | D | |
| X | CO2 | HCl | NaOH | AlCl3 |
| Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
- A.A
- B.B
- C.C
- D.D
 将物质X逐渐加入(或滴入)Y溶液中,其生成沉淀的量与加入X的物质的量关系如下图所示,符合图示情况的是
将物质X逐渐加入(或滴入)Y溶液中,其生成沉淀的量与加入X的物质的量关系如下图所示,符合图示情况的是| A | B | C | D | |
| X | CO2 | HCl | NaOH | AlCl3 |
| Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |