某含镍(Ni)废催化剂中主要含有Ni,还含有Al、Al2O3、Fe及其他不溶于酸、碱的杂质.部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下:
| 沉淀物 | Al(OH)2 | Fe(OH)3 | Fe(OH))2 | Ni (OH)2 |
| PH | 5.2 | 3.2 | 9.7 | 9.2 |
欲从含镍废催化剂中制得NiSO4?7H2O晶体,其流程如下:
请根据以上信息和流程图,回答下列问题:
(1)“碱浸”的目的是除去含镍废催化剂中的______.
(2)“酸浸”时所加入的酸是_______.酸浸后,滤液②中可能含有的金属离子是______.(用离子符号表示).
(3)“调pH为2-3的目的是______.
(4)步骤A的操作顺序是加热浓缩、冷却、______、______.
(5)NiSO4在强碱溶液中用NaC1O氧化,可制得碱性镍镉电池电极材料NiOOH.该反应的离子方程式为______.
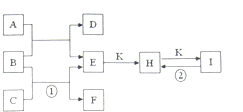 如图是常见的一些单质及其化合物之间的转化关系图.常温常压下,D、F、K均为无色无刺激性气味的气体,C为活泼的金属单质,B是最常见的无色液体,A是有单质C在D中燃烧生成的淡黄色固体,I是焙制糕点所用的发酵粉的主要成分之一.(反应中生成的部分物质已略去)
如图是常见的一些单质及其化合物之间的转化关系图.常温常压下,D、F、K均为无色无刺激性气味的气体,C为活泼的金属单质,B是最常见的无色液体,A是有单质C在D中燃烧生成的淡黄色固体,I是焙制糕点所用的发酵粉的主要成分之一.(反应中生成的部分物质已略去) 用如图所示的装置分别进行如下实验,各离子方程式书写正确且各组物质反应后溶液的导电性变化不大
用如图所示的装置分别进行如下实验,各离子方程式书写正确且各组物质反应后溶液的导电性变化不大
