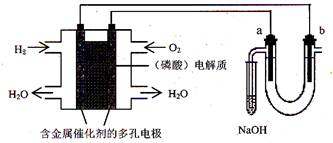
(10分)FeCl3可作印刷电路铜板腐蚀剂,反应的方程式为 2FeCl3+Cu=2FeCl2+CuCl2。
(1)将上述反应设计成的原电池如下左图所示,请回答下列问题:
①电极X的材料是 ;电解质溶液Y是 。
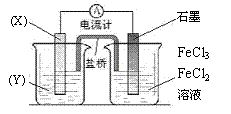 |  | ||
②X电极上发生的电极反应式为 。
(2)腐蚀铜板后的废腐蚀液中,含有FeCl3、FeCl2、CuCl2等物质,用电解法可回收铜且得到FeCl3溶液,其工作原理如上右图所示。请回答下列问题:
①该电解槽阴极的反应式是 、 。
②阴离子交换膜中通过的离子主要是 ,FeCl3溶液从出口 (填写 “A”或“B”)导出。
(10分)工业含铬(Cr)废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为沉淀。废水pH与Cr2O72-转化为Cr3+的关系如图1,实验室模拟工业电解法处理含铬废水的装置如图2:

请根据以上知识回答下列问题:
⑴ 含铬废水预处理的方法是 。
⑵ 在图2中连接铁棒的一极是电源的 极。
⑶ 实验中除能观察到废水颜色发生变化外,还能观察到的现象是 。
表一:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cr(OH)3 | Al(OH)3 |
| 开始沉淀 | 2.7 | 7,5 | 4.3 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 5.6 | 5.2 |
⑷ 当废水颜色不再发生明显变化时,切断电源,取出电极,再调节电解液的pH至8左右。调节pH的目的是 。
⑸ 含铬废水国家排放标准为![]() 含量≤0.1000mg/L。取上述电解后的废水200.00mL,调节pH=1后置于锥形瓶中,用浓度为0.0001mol/L的KI溶液滴定,至滴定终点时,用去KI溶液9.00mL。已知酸性条件下,I-被Cr2O72-氧化的产物为I2。用计算所得数据说明上述电解法处理后的废水是否符合国家排放标准 。
含量≤0.1000mg/L。取上述电解后的废水200.00mL,调节pH=1后置于锥形瓶中,用浓度为0.0001mol/L的KI溶液滴定,至滴定终点时,用去KI溶液9.00mL。已知酸性条件下,I-被Cr2O72-氧化的产物为I2。用计算所得数据说明上述电解法处理后的废水是否符合国家排放标准 。
(9分)某地有软锰矿和闪锌矿两座矿山,它们的组成如下:软锰矿:MnO2含量≥65%, SiO2含量约20%,Al2O3含量约4%,其余为水分;闪锌矿:ZnS含量≥80%,FeS、CuS、SiO2含量约7%,其余为水分。科研人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如下图所示。
|
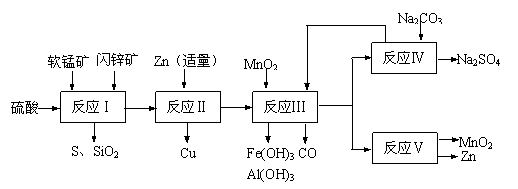
请回答下列问题:
(1)反应Ⅰ后过滤所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等。试写出反应Ⅰ中生成CuSO4的化学方程式 ▲ 。
(2)反应Ⅱ加入适量锌的作用是 ▲ 。如果锌过量,还会进一步发生反应的离子方程式为 ▲ 。
(3)反应Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为 ▲ 。
(4)本工艺所用的原料除软锰矿、闪锌矿、硫酸外还需要的原料是 ▲ 。
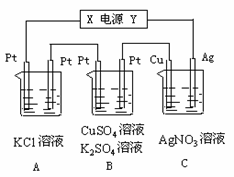 如图所示,若电解5min时铜电极质量增加2.16g,B池的两极都有气体产生。
如图所示,若电解5min时铜电极质量增加2.16g,B池的两极都有气体产生。