相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2 (g)+3H2(g)![]() 2NH3(g) △H=- 92.4 kJ/mol。
2NH3(g) △H=- 92.4 kJ/mol。
实验测得起始、平衡时的有关数据如下表:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
下列叙述正确的是 ( )
A.放出热量关系:a<b< 92.4
B.反应的平衡常数:③>①>②
C.达平衡时氨气的体积分数:①>③
D.N2的转化率:②>①>③
已知:C(s)+CO2(g)![]() 2CO(g);DH>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是
2CO(g);DH>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是
A.升高温度和减小压强 B.降低温度和减小压强
C.降低温度和增大压强 D.升高温度和增大压强
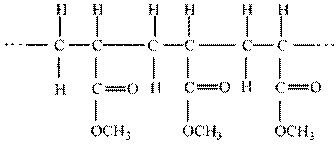
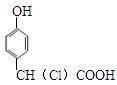 B.CH2(CHO)-CH2-CH(OH)-COOH
B.CH2(CHO)-CH2-CH(OH)-COOH