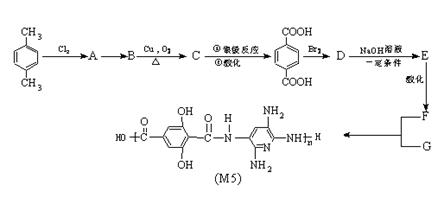
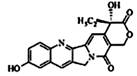
下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是( )
| 编号 | 化学反应 | 离子方程式 | 评价 |
| ① | 硫酸溶液中加入Ba(OH)2溶液 | Ba2++SO=BaSO4↓ | 正确 |
| ② | 氧化铝与NaOH溶液反应 | 2Al3++3O2-+2OH-= 2AlO+H2O | 错误,Al2O3不应写成离子形式 |
| ③ | 铁和稀硝酸反应 | Fe+2H+===H2↑+Fe2+ | 正确 |
| ④ | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br | 错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | 能形成双原子分子,原子间存在3对共用电子对 |
| X | M层有3个电子 |
| Y | 最外层电子数是最内层电子数2倍,其最高价氧化物是一种固体,用于生产光导纤维 |
| Z | 最低负价为—2价,且无最高正价 |
用化学符号回答以下问题:
(1) 比较:氢化物的稳定性:T Z,最高价氧化物对应水化物的酸性:T Y。(填“>”、“<”或“=”)
(2)Y元素位于元素周期表中第 周期,第 族。
请你设计一实验方案,证明X的氯化物是离子化合物还是共价化合物。简要写出实验内容、现象和结论。 。
(3)X的最高价氧化物对应水化物与烧碱反应的离子方程式为: 。
(4)T、X、Y、Z四种原子的半径由大到小的顺序为: 。