25℃时,几种弱酸的电离常数如下:
| 弱酸化学式 | CH3COOH | HCN | H2S |
| 电离常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1= 1.3×10-7 K2= 7.1×10-15 |
25℃时,下列说法正确的是
A. 等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN)
B. a mol/L HCN溶液与b mol/L NaOH溶液等体积混合,所得溶液中c(Na+)> c(CN-),则a一定大于b
C. NaHS和Na2S混合溶液中,一定存在c(Na+)+ c(H+)== c(OH-)+ c(HS-)+2c(S2-)
D. 某浓度HCN的水溶液pH=d,则其中c(OH-)=10-d mol/L
用下图装置进行实验,下表中实验结果能说明结论的是( )
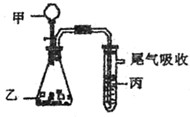
| 甲 | 乙 | 丙 | 结论 | |
| A. | 水 | 电石 | 溴水 | 稳定性:水>C2H2>Br2 |
| B. | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| C. | 盐酸 | FeS | 溴水 | 还原性:S2—>Br—>Cl— |
| D. | 浓盐酸 | KMnO4 | KBr溶液 | 氧化性:Cl2> KMnO4 >Br2 |