某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:(已知硅不溶于盐酸)
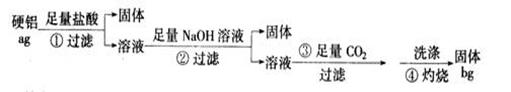
(1)补全上述①②③④各步反应的离子方程式
①Mg+2H+===Mg2++H2↑ ,___________________________
②_______________________, _______________________
Mg2++2OH-===Mg(OH)2↓
③ ___________________________________
CO2+H2O+ A1O2-===Al(OH)3↓+3HCO3-
|
④2A1(OH)3===Al2O3+H2O
(2)该样品中铝的质量分数是
(3)第②步中加入NaOH溶液不足时,会使测定结果 ,第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果 ,第④步对沉淀灼烧不充分时,会使测定结果 。(填“A”、“B”或“C”)
A.偏高 B.偏低 C.不影响
下列关于相同质量的N2O4(四氧化二氮)和NO2的说法中,正确的是( )
A. 物质的量之比为2:1 B. 物质的量之比为1:2
C. 氧原子的物质的量之比为2:1 D. 氧原子的物质的量之比为1:1

