0 36019 36027 36033 36037 36043 36045 36049 36055 36057 36063 36069 36073 36075 36079 36085 36087 36093 36097 36099 36103 36105 36109 36111 36113 36114 36115 36117 36118 36119 36121 36123 36127 36129 36133 36135 36139 36145 36147 36153 36157 36159 36163 36169 36175 36177 36183 36187 36189 36195 36199 36205 36213 203614
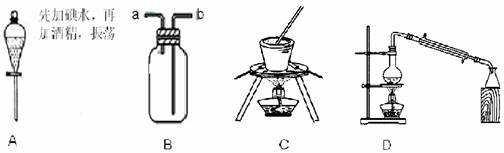

 (5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如右装置简图,请你参与分析讨论:
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如右装置简图,请你参与分析讨论: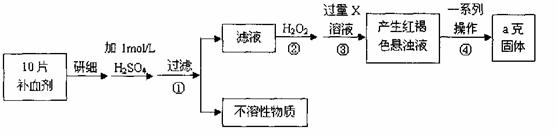 (5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。