0 34567 34575 34581 34585 34591 34593 34597 34603 34605 34611 34617 34621 34623 34627 34633 34635 34641 34645 34647 34651 34653 34657 34659 34661 34662 34663 34665 34666 34667 34669 34671 34675 34677 34681 34683 34687 34693 34695 34701 34705 34707 34711 34717 34723 34725 34731 34735 34737 34743 34747 34753 34761 203614
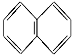 ,则萘的分子式为________,若萘分子中有一个氢原子被氯原子取代,另有一个氢原子被溴原子取代,所形成的化合物种类有_________种;若萘分子中有2个氢原子被溴原子取代,所形成的化合物种类有_______种。
,则萘的分子式为________,若萘分子中有一个氢原子被氯原子取代,另有一个氢原子被溴原子取代,所形成的化合物种类有_________种;若萘分子中有2个氢原子被溴原子取代,所形成的化合物种类有_______种。 C的结构单元。B分子比A分子多了几个这样的结构单元( )
C的结构单元。B分子比A分子多了几个这样的结构单元( )