实验组 | 温度 | 起始量 | 平衡量 | 达到平衡所需时间 | ||
H2O | CO | H2 | CO | |||
1 | 1 mol | 2 mol | 0.8 mol | 1.2 mol | 5 min | |
2 | 0.5 mol | 1 mol | 0.2 mol | 0.8 mol | 3 min | |
3 | a | b | c | d | t | |
(1)①由以上数据,实验1中以v(CO2)表示的反应速率为___________。
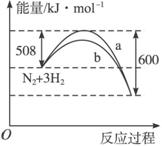
②该反应在
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t<3 min,则a、b应满足的关系是___________。
(2)下图1、2表示上述反应在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化的情况:

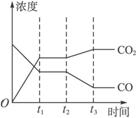
图1 图2
①图1中时刻t2发生改变的条件可能是________________________(写一条即可,下同)。
②图2中时刻t2发生改变的条件可能是__________________________________________。
(3)在

| C | D | G |
起始组成/mol | 6 | 4 | 0 |
某时刻组成/mol | 3 | 3 | 2 |
(1)若X由M、N两种短周期且同周期元素组成,M原子的最外层电子数是最内层电子数的![]() ,N元素最高正价与它的负价代数和为6。反应④的数据如上表格所示。
,N元素最高正价与它的负价代数和为6。反应④的数据如上表格所示。
①写出反应②的离子方程式________________________。
②物质G的水溶液中离子浓度由大到小的顺序为____________。
(2)若X是一种含氧酸盐,且B是一种过渡元素的金属,反应①所得B、C的物质的量之比为4∶1,反应②不需特定的反应条件就能进行,且A的浓度不同,产物E不同,则X物质的化学式可能是_______________。
(3)若X是一种含氧酸盐,B是金属单质,C、D是非金属单质,反应②需要B与A的浓溶液共热才能进行,且生成的E与G是同一种物质。
写出反应①的化学方程式________________________________________________。
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂。
(1)若假设1成立,则实验现象是________________________。
(2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗?___________。简述你的理由(不需写出反应的方程式)__________________。
(3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是____________,写出发生反应的离子方程式________________________。
探究延伸
经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
(4)实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为_________。
(5)实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4·5H2O)。经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
开始沉淀pH | 6.0 | 7.5 | 1.4 |
沉淀完全pH | 13 | 14 | 3.7 |
实验室有下列试剂可供选择:A.氯水 B.H2O
实验小组设计如下实验方案:

试回答:
①试剂1为___________,试剂2为___________(填字母)。
②固体X的化学式为________________________。
③操作Ⅰ为________________________。