下列数据是对应物质的熔点(℃):
Na2O | NaCl | AlF3 | AlCl3 |
920 | 801 | 1291 | 190 |
BCl3 | Al2O3 | CO2 | SiO2 |
-107 | 2073 | -57 | 1723 |
据此作出的下列判断错误的是( )
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子能力越强,在所形成的分子中成为带负电荷的一方。
0 31255 31263 31269 31273 31279 31281 31285 31291 31293 31299 31305 31309 31311 31315 31321 31323 31329 31333 31335 31339 31341 31345 31347 31349 31350 31351 31353 31354 31355 31357 31359 31363 31365 31369 31371 31375 31381 31383 31389 31393 31395 31399 31405 31411 31413 31419 31423 31425 31431 31435 31441 31449 203614
下面是某些短周期元素的x值:
元素符号 | Li | Be | B | C | O | F |
x值 | 0.98 | 1.57 | 2.04 | 2.25 | 3.44 | 3.98 |
元素符号 | Na | Al | Si | P | S | Cl |
x值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析x值变化规律,确定Mg、N的x值范围:
___________<x (Mg)< ___________,___________<x (N)< ___________。
(2)推测x值与原子半径关系是___________。根据短周期元素的x值变化特点,体现了元素性质的___________变化规律。
(3)某有机化合物结构式为:
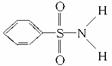 ,其中S—N键中你认为共用电子对偏向谁?________(写原子名称)。
,其中S—N键中你认为共用电子对偏向谁?________(写原子名称)。
(4)经验规律告诉我们:当成键的两原子相应元素的x差值(Δx)即x>1.7时,一般为离子键,Δx<1.7,一般为共价键,试推断:AlBr3中化学键类型是____________。
(5)预测元素周期表中,x值最小的元素的位置:____________(放射性元素除外)。
