在一密闭容器中充入1 mol NO2,建立平衡2NO2 N2O4,测得NO2的转化率为a%。在其他条件不变时,再充入1 mol NO2,待新平衡建立时,又测得NO2的转化率为b%,问a、b值的大小关系?
N2O4,测得NO2的转化率为a%。在其他条件不变时,再充入1 mol NO2,待新平衡建立时,又测得NO2的转化率为b%,问a、b值的大小关系?

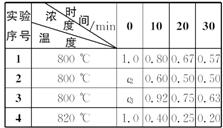
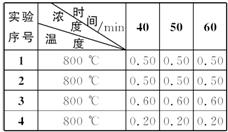
在密闭容器中,保持一定温度进行如下反应:N2(g)+3H2(g) 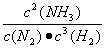 2NH3(g),已知加入1 mol N2和3 mol H2,在恒压条件下达到平衡时生成amol NH3,在恒容条件下达到平衡时生成b mol NH3(见表示编号①的一行)。若相同条件下,达到平衡时混合物中各组分的质量分数不变。回答下列问题:
2NH3(g),已知加入1 mol N2和3 mol H2,在恒压条件下达到平衡时生成amol NH3,在恒容条件下达到平衡时生成b mol NH3(见表示编号①的一行)。若相同条件下,达到平衡时混合物中各组分的质量分数不变。回答下列问题:
0 29836 29844 29850 29854 29860 29862 29866 29872 29874 29880 29886 29890 29892 29896 29902 29904 29910 29914 29916 29920 29922 29926 29928 29930 29931 29932 29934 29935 29936 29938 29940 29944 29946 29950 29952 29956 29962 29964 29970 29974 29976 29980 29986 29992 29994 30000 30004 30006 30012 30016 30022 30030 203614
(1)写出该反应的化学平衡常数表达式:K=__________________。
(2)平衡常数K值越大,表明建立平衡时_______________(填序号)。
A.N2的转化率越高 B.NH3的产量越大
C.正反应进行得越彻底 D.化学反应速率越快
(3)a与b的关系是:a_______________b(填“>”“<”或“=”)。
(4)填写下表:
状态 条件 | 起始时物质的物质的量(mol) | 平衡时NH3的物质的量(mol) | |||
编号 | X(N2) | Y(H2) | Z(NH3) | ||
恒容 | ① | 1 | 3 | 0 | b |
② | 0 | 0 |
| b | |
③ |
| 2.25 |
| b | |