(08黄埔区4月模拟)“碘钟”实验中,3I-+![]() →I3- +2SO42 -的反应速率可以用I3- 与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
→I3- +2SO42 -的反应速率可以用I3- 与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
实验编号 | ① | ② | ③ | ④ | ⑤ |
c(I-)/ mol?L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
c( | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
(1) 该实验的目的是___________________________________________________。
(2) 显色时间t1=______________。
(3) 温度对该反应的反应速率的影响符合一般规律,若在40 ℃下进行编号③对应浓度的实
验,显色时间t2的范围为______(填字母)。
a.<22.0 s b.22.0 s~44.0 s c.>44.0 s d.数据不足,无法判断
(4) 通过分析比较上表数据,得到的结论是_______________________________________。
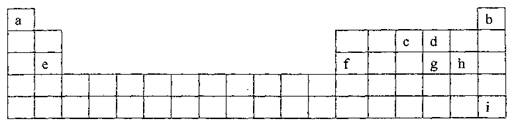
(08上海12校第二次联考)(A)下表是元素周期表的一部分,其中所列字母分别代表某一元素。
|
请你根据表中所给元素,回答下列问题:
(1)cdgh元素的氢化物中,沸点最高的是 (填该分子的电子式)。
(2)比较e、f单质及ef形成的合金,三者硬度由大到小的顺序 (填写名称)
(3)原子核外s电子总数比p电子总数少4个元素为 (填写元素符号),学习该元素低价氧化物的化学性质时,你可从三方面去把握;
①依据物质的类别,可知该氧化物属于 ;
②依据元素的化合价,可知该氧化物具有 ;
③将该氧化物通入 溶液中,使该溶液褪色,该氧化物具有 性。
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重大贡献的化学家莫瓦桑,你认为最先用来与F2反应制备稀有气体化合物的元素是 (填写元素符号)。
(5)用来组成酸、碱、盐三类物质至少需要的元素有 (填写表中字母)。(08闵行区模拟) A、B、C、D、E、F是原子序数依次增大的六种常见元素,其性质如下:
元素 | 性 质 |
A | 单质在C2中燃烧可生成AC和AC2两种气体 |
D | 原子的最外层电子与其最内层电子数相同 |
E | 单质在C2中燃烧的产物可使品红溶液褪色 |
F | 与C元素形成的化合物F3C4具有磁性 |
请回答下列问题:
(1)F元素在周期中的位置是 。
(2)AC2的结构式为 ;DC的电子式为 。
(3)元素C与元素E相比,非金属性较强的是 (用元素符号表示),能证明这一事实的是 。
(4)A、B、C形成的10电子氢化物中,热稳定性最好的是 (写化学式);B、C的氢化物分子结合H+能力较强的是 (写化学式),用离子方程式加以说明 。
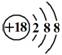 D.CH4分子的比例模型:
D.CH4分子的比例模型: