国家环保总局在2009年12月25日发布的重点城市空气质量日报的部分内容如下:
| 城市 | 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 |
| 北京 | 500 | 可吸入颗粒物 | V | 重污染 |
| 石家庄 | 80 | 二氧化硫 | II | 良 |
| 哈尔滨 | 97 | II | 良 |
下列说法错误的是
A.哈尔滨市的首要污染物通常为可吸入颗粒物
B.大气中的二氧化硫主要来自于火山喷发
C.空气质量与季节有关,冬季北方燃煤若不经处理,即会导致SO2含量的增加
D.首要污染物除二氧化硫,还可能有二氧化氮,二者都会引起酸雨的形成
据报道双氧水接触银能剧烈反应,为消除用硝酸清洗试管内壁上的银时产生的有毒气体污染环境,体现“绿色化学”的理念,某学校活动小组利用该反应清洗试管内壁上的银,并进一步研究反应的机理。他们查阅资料(资料信息:硝酸氧化性比过氧化氢强,能氧化过氧化氢;碘化银为黄色固体;稀硝酸与银单质反应条件为加热),设计并完成了以下实验。
第一步 清洗: 取10 mL 10% H2O2溶液清洗附有银的试管。反应剧烈,并产生大量的气体(经验证为氧气),试管内壁上的银全部被清除干净,最后得澄清透明液体a。用激光照射液体a能看到丁达尔效应。
第二步 探究反应原理: 取2支试管,分别取液体a约1 mL,稀释至3 mL得液体b。
学生甲:将1支盛有液体b的试管进行如下实验
 |
学生乙:向液体b中加入4~5滴稀硝酸酸化的2 mol/LNaCl溶液,溶液中出现白色沉淀。
通过上述实验,他们认为H2O2氧化了银单质。
请回答:
(1)液体a在分散系分类中属于 。
(2)操作x名称是 。
(3)学生甲在液体b中加入碘化钾溶液,没有看到预期的黄色的碘化银沉淀,可能的原因是
(填序号)。
①液体a中的银元素大多数以银单质的形式存在
②过量的H2O2将I―氧化为I2
③加入的碘化钾溶液量太少
(4)学生乙在实验中加入4~5滴稀硝酸酸化的原因是 。
(5)为探究银与H2O2反应生成的物质是否会对H2O2的分解有催化作用。进一步完成下列实验。
向1 mL 1mol/LAgNO3溶液中加入1滴 2 mol/L NaOH溶液,出现棕色沉淀,继续加入3mL10% H2O2溶液产生大量的气体。
①该实验并不能达到实验目的,还需要做对比实验,请设计对比实验的方案: 。
②如果银与H2O2反应生成的物质对H2O2的分解有催化作用,通过实验和理论上分析可以得到,起催化作用的物质是 。
实验室可由多条途径得到SO2。
(1)Na2SO3溶液与硫酸反应可以制得SO2,其离子方程式为 。
(2)铜与浓硫酸反应可以制得SO2,其化学方程式为 。
(3)如果要在实验室制取SO2,选用上述两种方法中的哪种更合理,你的理由是
。
(4)海波(Na2S2O3?5H2O)也能与硫酸反应制得SO2(Na2S2O3+ H2SO4= Na2SO4+ SO2↑+S↓+H2O )。工业制得的海波中可能含有Na2SO3。取三份质量不同的样品,分别加入40mL浓度相同的硫酸溶液后,过滤出硫黄,微热使SO2全部逸出,测得实验数据如下表(气体体积已换算为标准状况)。
第一份 | 第二份 | 第三份 | |
样品质量 | 10.00 | 20.00 | 40.00 |
SO2体积(L) | 0.448 | 0.896 | 1. 12 |
硫的质量 | 0.480 | 0.960 | 1.28 |
试计算:
①硫酸溶液的物质的量浓度是 mol/L。
②样品中n(Na2S2O3?5H2O):n(Na2SO3)= 。
燃料电池具有广阔的发展前途,科学家近年研制出一种微型的燃料电池,采用甲醇取代氢气做燃料可以简化电池设计,该电池有望取代传统电池。某学生在实验室利用碱性甲醇燃料电池电解Na2SO4溶液。
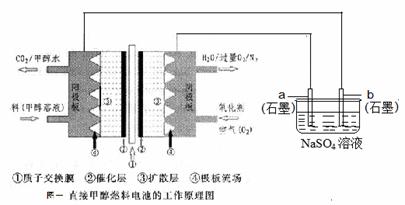 |
请根据图示回答下列问题:
(1)图中a电极是 (填“正极”、“负极”、“阴极”或“阳极”)。该电极上发生的电极反应式为 。
(2)碱性条件下,通入甲醇的一极发生的电极反应式为 。
(3)当消耗3.36 L 氧气时(已折合为标准状况),理论上电解Na2SO4溶液生成气体的总物质的量是
。
(4)25℃、101kPa时,燃烧16g甲醇生成CO2和H2O(l),放出的热量为363.26kJ,写出甲醇燃烧的热化学方程式: 。
“84消毒液”与硫酸溶液反应可以制取氯气(NaClO+ NaCl+H2SO4 = Na2SO4 + Cl2↑+H2O)
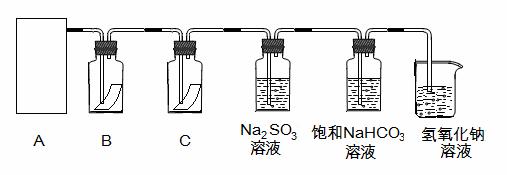
为探究氯气的性质,某同学设计了如下所示的实验装置
 |
请回答:
(1)从①、②、③装置中选择合适的制气装置(A处) (填写序号)。
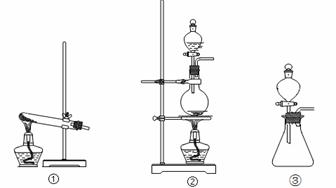
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是 ,说明该装置存在明显的缺陷,请提出合理的改进的方法 。
(3)为了验证氯气的氧化性,将氯气通Na2SO3溶液中,写出氯气与Na2SO3溶液反应的离子方程式 。
(4)氯气通入饱和NaHCO3溶液能产生无色气体,已知酸性盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有 。
(5)写出氯气与氢氧化钠溶液反应的化学方程式 ,为验证尾气吸收后的溶液中存在氯离子,正确的操作为 。
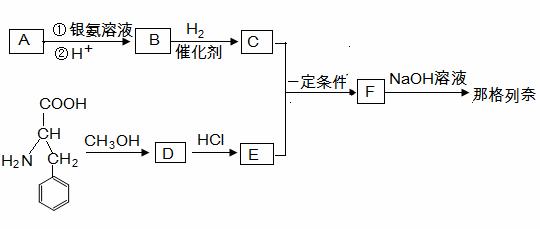
那格列奈是一种新型的餐时血糖调节剂,适用于2型糖尿病。其合成路线如下:
 |

已知:
 |
请回答:
(1)有机物A蒸气密度是相同状态下氢气密度的74倍,A分子中碳元素的质量分数是氢元素质量分数的10倍,A的1个分子中含有1个氧原子, A中含氧官能团的名称为 ;A的分子式为 。
(2)A的结构满足以下条件:
① 含有苯环,苯环上有两个取代基
② 苯环上的一溴取代物只有两种
③ 取代基上有三种不同的氢
写出A的结构简式: 。
(3)写出流程中制取D的化学方程式 。
(4)由F制取那格列奈的反应类型是 。
(5)1 mol B与3 mol H2加成得到C,写出由C和E制取F的化学方程式: 。
(6)物质B分子的取代基上一个氢原子被1个溴原子取代后,再消去1 个HBr得到G,下列关于G的说法正确的是 。
① 能使酸性高锰酸钾溶液褪色
② 核磁共振氢谱有7种类型氢原子的吸收峰
③ 能与碳酸氢钠反应放出气体
④ B经上述过程可以得到两种同分异构体
乙醇在浓硫酸作用下制取乙烯时,浓硫酸容易使乙醇碳化,用氧化铝替代浓硫酸重新设计实验如下。
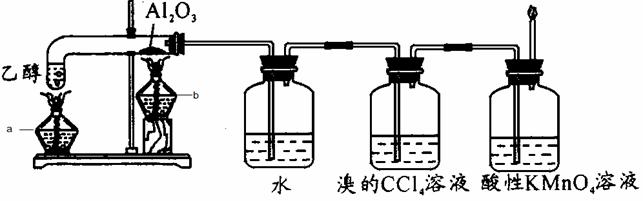 |
请回答:
(1)开始加热时应先点燃酒精灯 (填“a”或“b”)。
(2)水的作用是 ,可以将该瓶中收集到的物质分离的常用方法是 。
(3)可利用 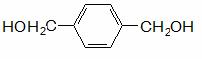 和乙烯合成世界上产量最大的合成纤维(PET),
和乙烯合成世界上产量最大的合成纤维(PET),
其结构简式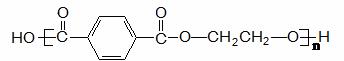 。
。
按下列示例写出和乙烯合成PET的反应流程图(其他原料自选,并注明必要的反应条件)。
反应流程图例如:![]()
![]()
![]()
![]()
![]() -Br
-Br
下图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。
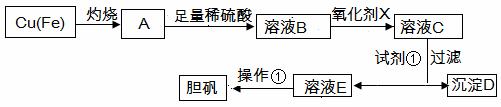 |
已知:
| 溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
请回答:
(1)溶液B中含有的阳离子有 (填离子符号)。
(2)下列物质中最适宜做氧化剂X的是 (填字母)。
a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,试剂①可以选择 (填化学式)。
(4)操作①的名称是 。
(5)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是
a.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
b.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
c.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
d.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(6) 沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉,其原因是
(用离子方程式表示),还需要加入过量的盐酸,原因是 。