为探索工业含铝、铁、铜合金废料的再利用,某同学实设计的实验方案如下:

(1)操作①用到的玻璃仪器有_______________________________________;
(2)写出反应①的化学方程式_______________________________________;
反应②的离子方程式___________________________________________;
(3)设计实验方案,检测滤液D中含有的金属离子(试剂自选)__________;
(4)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无
色液体,反应④的总化学方程式是______________________________________;
(5)将滤渣B的均匀混合物平均分成四等份,每份13.2g,分别加入同浓度的稀硝酸,充分反应后,在标准状况下生成NO的体积与剩余金属的质量见下表(设硝酸的还原产物只有NO)。
| 实验编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属质量/g | 9.0 | 4.8 | 0 | 0 |
| NO体积/L | 1.12 | 2.24 | 3.36 | V |
试通过计算填空:
①写出实验①中发生反应的离子方程式__________________________;
②实验④中V=____________________________。
有关元素X、Y、Z、D、E的信息如下:
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期叙述之差为4 |
| Z | 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物,能按1:1电力出电子数相等的阴、阳离子 |
| E | 其单质有多中同素异形体,一种为自然界中硬读最大 |
(1)画出Y的离子结构示意图_________________________;
(2)写出D的最高4氧化物的水化物电离出的阴离子的电子式_________;
(3)![]() 的溶液与Y的单质可能发生反应,其反应的离子方程式为__________;
的溶液与Y的单质可能发生反应,其反应的离子方程式为__________;
(4)用化学符号表示,![]() 的水溶液中各离子的浓度关系________(列等式);
的水溶液中各离子的浓度关系________(列等式);
 (5)已知
(5)已知![]() 与
与![]() 可发生反应
可发生反应
![]() ;当反应达到
;当反应达到
平衡时不断改变条件(不改变![]() 、
、![]() 、
、![]() 的量)反
的量)反
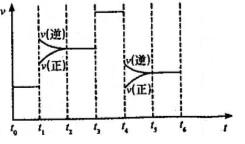
应速率随时间的变化如右图:其中表示平衡混合物中![]()
含量最高的一段时间是___________;如![]() 平衡常数为
平衡常数为
![]() 平衡常数为
平衡常数为![]() ,则
,则![]() ________
________![]() (填“大于”、
(填“大于”、
“等于”或“小于”)。
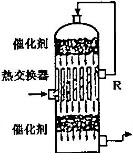 (2)在硫酸工业生产中,为了有利于
(2)在硫酸工业生产中,为了有利于