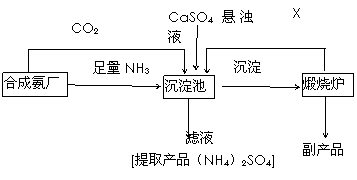
对羟基苯甲醛是一种合成医药、香料、液晶材料的重要中间体,以对甲基苯酚( ![]() ) 为主要原料合成对羟基苯甲醛
) 为主要原料合成对羟基苯甲醛
( ![]() ) 的工艺 流程如图所示。
) 的工艺 流程如图所示。
 |
(1)写出反应Ⅱ化学方程式____________________________________________,
B能跟银氨溶液反应生成银,写出该反应的化学方程式____________________
_________________________________________________
(2)在生产中不直接用氧气氧化对甲基苯酚的原因是_______________________________
____________________________________________
(3)写出对羟基苯甲醛在一定条件下与足量氢气反应的化学方程式
___________________________________________________________
(4)对羟基苯甲醛有多种同分异构体,其中苯环上只有一个侧链的同分异构体的结构简式为______________________________________________.
某固体混合物可能由Al 、(NH4)2SO4、MgCl2 、FeCl2 、AlCl3 中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
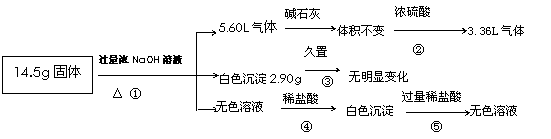
回答下列问题:
(1)写出反应④的离子方程式___________________________________________.
(2)填写下表中的空白。(注:若混合物中不存在该成分,则“质量”栏中填“0”;
画斜线的表格不需填写)
| 成分 | 质量 | 判断依据或计算推理过程 |
| Al | ||
| (NH4)2SO4 | ||
| MgCl2 | ||
| FeCl2 | ||
| AlCl3 |
I.如下图所示,将2molA气体和1molB气体充入一容积可变的密闭容器中。
发生反应:2A(g)+B(g)![]() 2C(g)。反应开始时可滑动的活塞的位置如图1所示,当反应达到平衡时,活塞位置如图2所示.则达到平衡时,A的转化率为________________;
2C(g)。反应开始时可滑动的活塞的位置如图1所示,当反应达到平衡时,活塞位置如图2所示.则达到平衡时,A的转化率为________________;
该条件下反应的平衡常数为_______________________________。
|
|

|
|
|
|
|
Ⅱ.(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3KJ。写出该反应的化学方程式__________________________________________.
 (20利用该反应设计一个燃料电池:用氢氧化钾溶液做电解 质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式____________________________
(20利用该反应设计一个燃料电池:用氢氧化钾溶液做电解 质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气。写出负极的电极反应式____________________________
![]() (3)有如右化学实验装置图,
(3)有如右化学实验装置图,
石墨棒上的电极反应式为_______________________________;
如果起始时盛有1000mLpH=5的硫酸铜溶液(25℃)(CuSO4 足量),一段时间后溶液的pH变为1,若要使溶液恢复到起始浓度(忽略溶液体积的变化),可向溶液中加入________(填物质名称),其质量为_______________.
下列表格中的各种情况,可以用右侧的图象曲线表示的是
|
| 反应 | 纵坐标 | 甲 | 乙 |
| A | 相同质量氨,在同一容器中2NH3 | 氨气的转化率 | 500℃ | 400℃ |
| B | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
| C | 在体积可变的恒压容器中,体积比1:3的 | 氨气的浓度 | 活性高的 催化剂 | 活性一般的 催化剂 |
| D | 2mol SO2 与1molO2,在相同温度下 | SO3物质的量 | 10个 大气压 | 2个大气压 |