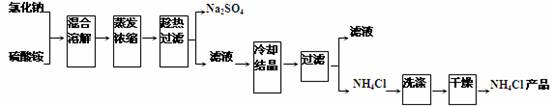
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:先配制100mL 0.10 mol?L-1 NaOH标准溶液,然后取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作3次,记录数据如下。
| 实验编号 | NaOH溶液的浓度 (mol?L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.02 | 20.00 |
| 2 | 0.10 | 21.92 | 20.00 |
| 3 | 0.10 | 22.06 | 20.00 |
①滴定达到终点的标志是___________________________________________
②根据上述数据,可计算出该盐酸的浓度_______________
③排去碱式滴定管中气泡的方法应采用操作_________________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

甲 乙 丙
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_____(多选扣分)
A.滴定终点读数时俯视读数
B.碱式滴定管尖嘴部分有气泡,滴定后消失
C.锥形瓶水洗后未干燥
D.锥形瓶水洗后用待测稀盐酸溶液润洗
E.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗