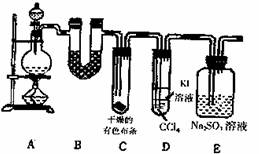
水煤气(主要成分:CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
C(s)+ H2O(g)![]() CO(g)+H2(g);△H =+131.3kJ•mol-1
CO(g)+H2(g);△H =+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。
| 容器 编号 | c(H2O)/mol?L-1 | c(CO)/mol?L-1 | c(H2)/mol?L-1 | V正、V逆比较 |
| I | 0.06 | 0.60 | 0.10 | V正=V逆 |
| II | 0.06 | 0.50 | 0.40 | ②? |
| III | 0.12 | 0.40 | 0.80 | V正<V逆 |
| IV | 0.12 | 0.30 | ①? | V正=V逆 |
请根据上表数据计算出该温度下该反应的平衡常数的数值
填写表中相应的空格① 、② ;
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mol水蒸气,发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍,平衡时水蒸气的转化率为 ;向该容器中补充 a mol 炭,水蒸气的转化率将 (填 “增大”、“减小”、“不变”)。
(3)已知:CO(g) + ![]() O2(g) =CO2 (g);△H =-283.0 kJ?mo1-1
O2(g) =CO2 (g);△H =-283.0 kJ?mo1-1
H2(g) + ![]() O2 (g) =H2O (g);△H = -241.8kJ?mo1-1
O2 (g) =H2O (g);△H = -241.8kJ?mo1-1
C(s) + ![]() O2(g)=CO (g);△H = -110.5kJ?mo1-1
O2(g)=CO (g);△H = -110.5kJ?mo1-1
那么,将12 g 炭完全转化为水煤气,然后再燃烧,整个过程放出 kJ的热量。
有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阳离子和一种阴离子且互不重复)
| 阳离子 | K+、Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO―、Cl―、OH―、SO42― |
已知:①A、C溶液的pH均大于7,B溶液的pH小于7,A、B的溶液中水的电离程度相同;D溶液焰色反应显黄色。
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A的名称是
(2)写出C溶液和D溶液反应的化学方程式
(3)25℃时pH=9的A 溶液和pH=9的C溶液中水的电离程度小的是 (填的A或C化学式);
(4)25℃时用惰性电极电解D的水溶液,一段时间后溶液的pH 7;(填>、< 或=)
(5)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为 ;
(6)室温时在一定体积0.2mol?L―1的C溶液中,加入一定体积的0.1mol?L―1的盐酸时,混合溶液的pH=13,若反应后溶液的体积等于C溶液与盐酸的体积之和,则C溶液与盐酸的体积比是 。
下列实验操作不正确的是( )
| 编号 | 实验 | 操作 |
| A | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,上层液体从分液漏斗上口倒出 |
| B | 配制一定浓度的氯化钾溶液1000mL | 准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容 |
| C | 鉴别NaCl溶液和KCl溶液 | 用焰色反应 |
| D | FeCl2是否已被氧化而变质 | 用KSCN溶液检验 |