(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示可逆反应的进行程度越大,K值大小与温度的关系是:温度升高,K值 (填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO (g) + H2O (g) ![]() CO2 (g) + H2 (g) △H<0
CO2 (g) + H2 (g) △H<0
CO和H2O浓度变化如下图,则O―4min的平均反应速率v (CO) = mol / (L?min)
|
|
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3 min―4min之间反应处于 状态;
C1数值 0.08mol / L(填大于、小于或等于)。
②反应在4 min―5min间,平衡向逆方向移动,可能的原因是 (单选),
表中5 min―6min之间数值发生变化,可能的原因是 (单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
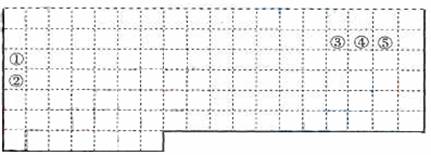
下表中的实线表示元素周期表的部分边界。①―⑤分别表示元素周期表中对应位置的元素。
|
(1)请在上表中用实线补全元素周期表边界。
(2)元素⑤的原子核外p电子数比s电子总数多 个,元素③氢化物的电子式为 。
(3)元素④一般在化合物中显 价,但与 形成化合物时,所显示的价态则恰好相反。
(4)在元素①的单质、元素②的单质和元素①②形成的合金这三种物质中,熔点最低的是 。
a.元素①的单质 b.元素②的单质
c.元素①②形成的合金 d.无法判断


 是由二四基二氯硅烷
是由二四基二氯硅烷 经两种反应而制得的,这两种反应依次是 ( )
经两种反应而制得的,这两种反应依次是 ( )