Na2S2O3?5H2O(俗称海波)是照相业常用的一种定影剂,常采用下列方法制取:将亚硫酸钠溶液与硫硫粉混合共热,生成硫代硫酸钠(Na2SO3+S=Na2S2O3),滤去硫粉,将滤液浓缩、冷却,即有Na2S2O3?5H2O晶体析出。该法制得的晶体中常混有少量Na2SO3和Na2SO4杂质。
为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,分别加入相同浓度的H2SO4溶液20mL,充分反应后滤出硫,并将滤液微热(假定生成的SO2全部逸出),测得有关实验数据如下(标准状况):
| 第一份 | 第二份 | 第三份 | |
| 样品的质量(g) | 12.60 | 18.90 | 28.00 |
| SO2的体积(L) | 1.12 | 1.68 | 2.24 |
| 硫的质量(g) | 1.28 | 1.92 | 2.56 |
已知:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O
通过计算确定样品的成分及各成分的物质的量之比。
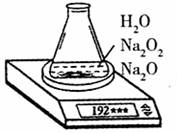
某种含有少量氧化钠的过氧化钠试样(已知试样质量为1.560g、锥形瓶和水的质量为190.720g),利用图示装置测定混合物中Na2O2的质量分数,每隔相同时间读得电子天平的数据如附表:
| ||||||||||||||||
| ||||||||||||||||
(1)写出Na2O2和H2O反应的化学方程式 。
(2)计算过氧化钠的质量分数时,必需的数据是 ;
不必作第6次读数的原因是 。
(3)测定上述样品(1.560g)中Na2O2质量分数的另一种方案,其操作流程如下:
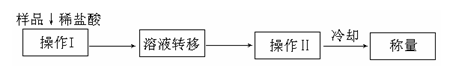
①操作Ⅱ的名称是 。
②需要直接测定的物理量是 。
③测定过程中需要的仪器有电子秤、蒸发皿、酒精灯,还需要 、 (固定、夹持仪器除外)。
④在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果 (填偏大、偏小或不变)。
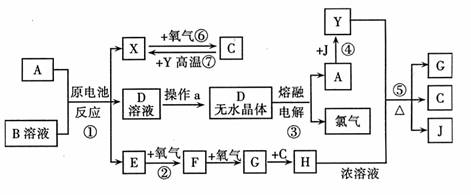
已知A为中学化学中的常见金属,X、Y为常见非金属,A、X、Y都位于周期表中短周期。其中A、Y常温下为固体,X、E、F、G、J常温下为气体,C为无色液体,B是一种盐,受热易分解,分解产物为E和HCl。现用A与石墨作电极,BCY的浓溶液作电解质,构成原电池。有关物质之间的转化关系如下图(部分反应的条件、生成物被略去):
|
请填写下列空白:
(1)金属A为 ;操作a是将D溶液在HCl气流中蒸干,
原因是 。
(2)反应②的化学方程式为: ;
反应⑤的化学方程式为: 。
(3)原电池反应①中,正极反应式为: 。