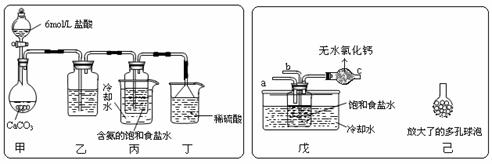
下图中每个方框表示有关的一种反应物或生成物,方框中字母是物质代号,已知B、D、E、F、X均为单质,试填空。
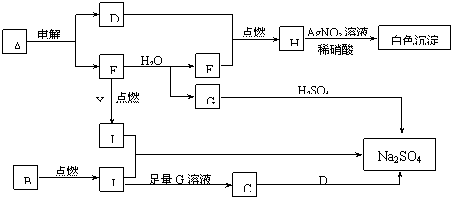 |
⑴写出A、B的化学:A___________,B____________。
⑵写出I和J反应的化学方程式__________________________________________。
写出E和水反应的离子方程式_________________________________________。
⑶写出C溶液和D反应的离子方程式_____________________________________。
 进行:
进行: