氰气[(CN)2]和氰化物都是剧毒性物质,氰分子的结构式为N≡C-C≡N,性质与卤素相似,下列叙述错误的是( )
| A、氰分子中四原子共直线,是非极性分子 | B、氰分子中C≡N键长大于C≡C键长 | C、氰气分子中含有σ键和π键 | D、氰分子在一定条件下能与烯烃发生加成反应 |
在单质及共价化合物的晶体中,一定不存在( )
| A、离子键 | B、共价键 | C、氢键 | D、分子间作用力 |
下表为元素周期表的一部分,有关说法正确的是( )
| 族 周期 |
IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| A、④、⑤、⑥、⑦、①的原子半径依次减小 |
| B、⑤、⑥、⑧的最高价氧化物对应的水化物不能相互反应 |
| C、⑦、②、③、④的氢化物的稳定性依次增强 |
| D、②、③的气态氢化物均能与它们的最高价氧化物对应的水化物反应 |
下表为元素周期表中短周期的一部分,下列有关A、B、C、D、E五种元素的叙述中,不正确是( )
| A | B | C | ||
| D | E | |||
| A、A能分别和B、E形成只含极性键的非极性分子 | ||||
| B、B、C分别形成的简单离子半径大小是:B大于C | ||||
| C、E的氢化物的沸点比C的氢化物的沸点高 | ||||
D、A与B形成的阴离子可能有:AB
|
下列有关物质结构的表述正确的是( )
A、次氯酸的电子式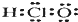 | B、二氧化硅的分子式SiO2 | C、二氧化碳的比例模型: | D、Cl-的结构示意图: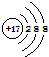 |
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A、次氯酸的电子式: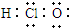 | B、质量数为16的氧原子:168O | C、乙炔的结构简式:H-C≡C-H | D、P4、CH4、NH4+ 粒子的空间构型均为正四面体型;CO2、C2H2均为直线型分子 |
下列化学用语和叙述正确的是( )
| A、乙二醛的分子式为:OHC-CHO | B、过氧化钙(CaO2)的电子式为: | C、表示稀硫酸和稀氢氧化钠溶液反应的“中和热”对应的热化学方程式:H2SO4(aq)+2NaOH (aq)=Na2SO4(aq)+2H2O(l);△H=-114.6kJ/mol | D、由C(石墨)=C(金刚石);△H=+119kJ/mol可知,金刚石不如石墨稳定 |
下列各组物质中,与O2和O3的关系相同的一组是( )
| A、Na和Na+ | ||||
| B、金刚石和C60 | ||||
C、
| ||||
| D、水和重水 |
在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是( )
| A、Na202+2H20=4NaOH+02 | B、CaC2+H20=Ca(OH)2+CH≡CH↑ | C、Mg3N2+6H20=3Mg(OH)2↓+2NH3↑ | D、NH4Cl+NaOH=NaCl+H20+NH3↑ |
2004年,美国科学家通过“勇气”号太空车探测出水星大气中含有一种称为硫化羰(化学式为COS)的物质,己知硫化羰的结构与二氧化碳相似,但能在氧气中完全燃烧,下列有关硫化羰的说法中正确的是( )
| A、硫化羰是酸性氧化物 | B、硫化羰是由极性键构成的非极性分子 | C、硫化羰可用做灭火剂 | D、硫化羰在氧气中完全燃烧后的生成物是CO2和SO2 |