以下变化后物质的总能量升高的是( )
| A、钢铁生锈 | B、气态SO3变成固态三聚物 | C、水电解 | D、1,3-环己二烯生成苯 |
下列事实不能用平衡移动原理解释的是( )
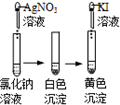 |
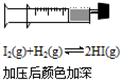 |
|
| ||||||||||||
| A | B | C | D |
| A、A | B、B | C、C | D、D |
在2L密闭容器中进行如下反应:N2+3H2
2NH3,5min内氨的质量增加了1.7g,则反应速率为( )
| ||
| 高温高压 |
| A、V(NH3)=0.02mol.(L.min)-1 |
| B、V(NH3)=0.01mol.(L.min)-1 |
| C、V(N2)=0.01mol.(L.min)-1 |
| D、V(H2)=0.03mol.(L.min)-1 |
在某一化学反应中,反应物A的浓度在20s内从1.0mol/L变为0.2mol/L,则在这20s内以A浓度的变化表示的平均反应速率为( )
| A、0.04 mol/(L?s) | B、0.04 mol/L | C、0.08 mol/(L?s) | D、0.08 mol/L |
在恒温下的定容密闭容器中,反应2SO2+O2?2SO3已经达到平衡状态的标志是( )
| A、容器中SO2、O2和SO3共存 | B、SO2和SO3的物质的量浓度相等 | C、反应器内压强不再变化 | D、容器中的SO2、O2、SO3的物质的量之比为2:1:2 |
某温度下,在一固定容积的密闭容器中进行下列反应:H2(g)+I2(g)?2HI(g),下
列情况一定能说明反应已达到限度的是( )
列情况一定能说明反应已达到限度的是( )
| A、正向反应的速率=逆向反应速率 | B、气体的总质量不再改变时 | C、容器内压强不再发生变化 | D、混合气体的总分子数不再改变 |
已知HI为无色气体,对于可逆反应H2(g)+I2(g)═2HI(g),下列叙述能够说明反应已达到平衡状态的是( )
| A、混合气体的颜色不再变化 | B、υ(H2)正=υ(HI)逆 | C、断裂2mol H-I键的同时生成1mol I-I键 | D、H2、I2、HI的物质的量浓度之比为1:1:2 |
对于可逆反应:N2+3H2?2NH3(正反应为放热反应),下列说法中正确的是( )
| A、反应达到平衡时,各物质的浓度不再发生变化 | B、反应达到平衡时,各物质的浓度都相等 | C、反应达到平衡时,各物质的浓度之比为1:2:3 | D、降低温度时,反应的正反应速率增大,而逆反应速率减小 |