室温下,对于0.10mol?L-1的氨水,下列判断正确的是( )
| A、与AlCl3溶液发生反应的离子方程式为Al3++3OH-═Al(OH)3↓ | B、加水稀释后,溶液中c(NH4+)?c(OH-)变大 | C、用HNO3溶液完全中和后,溶液不显中性 | D、其溶液的pH=13 |
从以下事实中找出不能应用勒夏特列原理解释的是( )
| A、温度过高对合成氨不利 | B、合成氨在高压下进行是有利的 | C、合成氨在高温下进行和加入催化剂都能使化学反应速率加快 | D、增大N2的浓度可提高平衡混合物中NH3的含量 |
COCl2(g)?CO(g)+Cl2(g);△H>0.当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
| A、①②④ | B、①④⑥ | C、②③⑤ | D、③⑤⑥ |
四个体积相同的密闭容器中在一定的条件下发生反应:2SO2+O2
|
下列说法正确的是( )
| A、纯水升高温度,电离平衡向正反应方向移动,Kw不变 | ||||
| B、在其它条件不变时,向H2(g)+I2(g)?2HI(g)平衡体系中加催化剂,反应速率加快,I2的转化率不变 | ||||
| C、pH=4的盐酸和氯化铵溶液分别加水稀释100倍,pH均变为6 | ||||
D、高铁电池:3Zn+2K2FeO4+8H2O
|
 用CO合成甲醇(CH3OH)的化学反应方程式为:
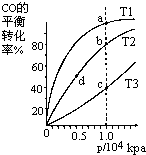
用CO合成甲醇(CH3OH)的化学反应方程式为:CO(g)+2H2(g)?CH3OH(g)△H<0按照相同的物质的量投料,测的CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
| A、平衡常数:K(a)>K(c),K(b)=K(d) | B、正反应速率:v(a)>v(c),v(b)>v(d) | C、平均摩尔质量:M(a)<M(c),M(b)>M(d) | D、平衡时a点一定有n(CO):n(H2)=1:2 |
在一定温度下,向容积不变的密闭容器中充入amolA,发生反应:2A(g)?B(g);△H<0.达平衡后再向容器中充入amolA,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
| A、相对平均分子质量增大 | B、A的转化提高 | C、V正增大,V逆减小 | D、反应放出的总热量大于原来的2倍 |
 如图表示反应X(g)?4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线.下列有关该反应的描述正确的是( )
如图表示反应X(g)?4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线.下列有关该反应的描述正确的是( )