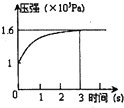
 一定温度下,向体积为2L的密闭容器中充入1mol PCl5(g),发生反应:PCl5(g)?PCl3(g)+Cl2(g)△H=+QkJ?mol-1 维持容器温度不变,测得容器内压强随反应时间的变化如图所示.下列说法正确的是( )
一定温度下,向体积为2L的密闭容器中充入1mol PCl5(g),发生反应:PCl5(g)?PCl3(g)+Cl2(g)△H=+QkJ?mol-1 维持容器温度不变,测得容器内压强随反应时间的变化如图所示.下列说法正确的是( )| A、3s内的平均速率为:v(PCl3)=0.1 mol?L-1?s-1 | B、达到平衡时放出0.6Q kJ热量 | C、其他条件不变,升高温度,平衡常数减小 | D、其他条件不变,再向容器中充入1mol PCl5(g),则达新平衡时,c(PCl5)>0.4mol?L-1 |
某反应A+B=C+D 在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确的是( )
| A、△H<0△S>0 | B、△H>0△S>0 | C、△H<0△S<0 | D、△H>0△S<0 |
已知反应2CO(g)═2C(s)+O2(g)的△H为正值,△S为负值.设△H和△S不随温度的改变而改变.则下列说法中,正确的是( )
| A、低温下是自发变化 | B、高温下是自发变化 | C、低温下是非自发变化,高温下是自发变化 | D、任何温度下是非自发变化 |
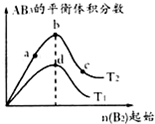 某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n 表示物质的量).下列判断正确的是( )
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n 表示物质的量).下列判断正确的是( )| A、在T2和n(A2)不变时达到平衡,AB3的物质的量大小 为:c>b>a | B、若T2>T1,则正反应一定是放热反应 | C、达到平衡时A2的转化率大小为:b>a>c | D、若T2>T1,达到平衡时b、d点的反应速率为vd>vb |
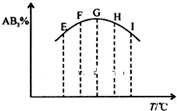 在容积相同的五个密闭容器中分别放入等量的A2和B2,在不同温度下同时任其发生反应:A2(g)+3B2(g)?2AB3(g),分别在某一同时刻测得其中AB3所占的体积分数变化如图所示,下列说法不正确的是( )
在容积相同的五个密闭容器中分别放入等量的A2和B2,在不同温度下同时任其发生反应:A2(g)+3B2(g)?2AB3(g),分别在某一同时刻测得其中AB3所占的体积分数变化如图所示,下列说法不正确的是( )| A、正反应是放热反应 | B、E、F二点尚未达到平衡 | C、H、I二点尚未达到平衡 | D、G、H、I三点已达平衡状态 |
已知,图一表示的是可逆反应CD(g)+H2(g)?C(s)+H20(g)△H>0的化学反应速率(c)与时间(t)的关系.图二表示的是可逆反应2NO2(g)?N2O4(g)△H<0的浓度(c)随时间(t)的变化情况,下列说法正确的是( )


| A、图一的t2时刻和图二的t1时刻改变的条件都有可能是升高了温度或增大了压强 | B、若图二t1时刻改变的条件是增大压强,则混合气体的平均相对分子质量将减小 | C、图一表示在新条件下达到平衡时V′(正)>V′(逆),图二表示在新条件下达到平衡时V′(正)<V′(逆) | D、其他条件不变,分别使用不同催化剂上述反应的平衡常数均不变 |
下列说法不正确的是( )
| A、常温下反应2Na2SO3(s)+O2(g)═2Na2SO4(s)能自发进行,则△H<0 | ||||
| B、Al2(SO4)3溶液蒸干所得固体产物为Al(OH)3 | ||||
| C、电解NH4Cl和HCl混合溶液在阴极可生成H2 | ||||
D、用碳酸钠溶液浸泡锅炉水垢:CO
|
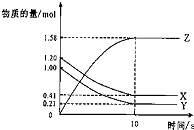 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是( )| A、反应开始到10s,用Z表示的反应速率为 0.158mol/(L?s) | B、反应开始到10s,X的物质的量浓度减少了0.79mol/L | C、反应开始到10s时,Y的反应速率为0.0395mol/(L?s) | D、反应的化学方程式为:X(g)+Y(g)?Z(g) |