镁-过氧化氢燃料电池具有比能量高、安全方便等优点,其结构示意图如图所示.该电池的总反应式为:Mg+H2O2+H2SO4=MgSO4+2H2O关于该电池的叙述正确的是( )
| A、该电池可以在高温下正常工作 | B、电池工作时,H+向正极移动 | C、电池工作时,正极周围溶液的pH将不断变小 | D、正极反应方程式为:H2O2+2H++2e-=2H2O |
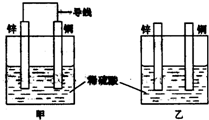 关于如图所示装置的叙述,正确的是( )
关于如图所示装置的叙述,正确的是( )| A、两装置中锌片都发生氧化反应 | B、两装置中溶液的pH均增大 | C、两装置中铜片的质量均逐渐减小 | D、两装置中铜片表面均无气泡产生 |
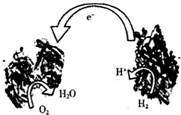 2006年,科学家发明了一种能够给电子设备提供动力的生物燃料电池.该电池的两个涂覆着催化剂酶的电极处于充满空气和少量氢气的玻璃槽中,总反应为:2H2+O2?2H2O,由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图.下列说法不正确的是( )
2006年,科学家发明了一种能够给电子设备提供动力的生物燃料电池.该电池的两个涂覆着催化剂酶的电极处于充满空气和少量氢气的玻璃槽中,总反应为:2H2+O2?2H2O,由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图.下列说法不正确的是( )| A、右边电极为该电池的负极 | B、该电池可以在高温环境下使用 | C、该装置为化学能转变为电能的装置 | D、该电池正极发生的是还原反应 |
下列叙述正确的是( )
| A、构成原电池的正极和负极必须是两种不同的金属 | B、铁与稀H2SO4反应时,加入少量CuSO4溶液,可加快化学反应速率 | C、在铁制的产品上电镀铜时,要用金属铜作阴极 | D、用惰性电极电解NaCl饱和溶液,溶液的pH值不变 |
目前市场上的手提应急灯,主要是“无液干粉”铅酸蓄电池,其原理是将有腐蚀性的浓硫酸灌注到硅胶凝胶中去,使电解质溶液不易发生泄漏,大大改善了电池的性能.所用的原料仍然是铅--二氧化铅--硫酸.下列关于该铅酸蓄电池的说法正确的是( )
| A、充电时电源的正极接蓄电池标“+”的一极 | B、“无液干粉”铅酸蓄电池彻底改变了原来的铅酸蓄电池的反应原理 | C、放电时在铅酸蓄电池的负极发生还原反应 | D、充电时铅酸蓄电池上标有“-”的电极发生氧化反应 |
 某兴趣小组设计如下微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一 段时间后,断开K1闭合K2,发现电流发A指针偏转.下列有关描述正确的是( )
某兴趣小组设计如下微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一 段时间后,断开K1闭合K2,发现电流发A指针偏转.下列有关描述正确的是( ) 下图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽.按下图接通电路后发现B上的c点显红色.为实现铁上镀锌,接通K后,使c、d两点短路.下列叙述正确的是( )
下图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽.按下图接通电路后发现B上的c点显红色.为实现铁上镀锌,接通K后,使c、d两点短路.下列叙述正确的是( )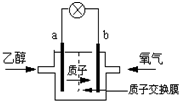 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( ) 如图是某空间站能量转化系统局部示意图,其中燃料电池采用KOH溶液作电解质.下列有关说法正确的是( )
如图是某空间站能量转化系统局部示意图,其中燃料电池采用KOH溶液作电解质.下列有关说法正确的是( )