短周期Y元素的p轨道上有3个未成对电子,则该元素的最高价氧化物的水化物的化学式可能是( )
| A、H3YO4 | B、H4YO4 | C、HYO2 | D、H2YO4 |
下列各项表述中与示意图一致的是( )
A、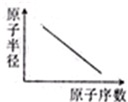 表示IA族元素原子半径的变化规律 | B、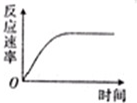 表示MnO2和热的浓盐酸反应时,反应速率随时间的变化 | C、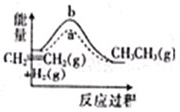 a、b曲线分别表示反应:CH2 CH2(g)+H2(g)→CH3CH3(g)△H<O在使用和未使用催化剂时,反应过程中的能量变化 | D、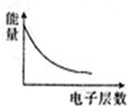 表示核外电子能量与电子层数的关系 |
X、Y为短周期元素,X位于 I A族,X与Y可形成化合物X2Y,下列说法正确的是( )
| A、X的原子半径一定大于Y的原子半径 | B、X2Y可能是离子化合物,也可能是共价化合物 | C、两元素形成的化合物中,原子个数比不可能为1:1 | D、X与Y的简单离子不可能具有相同的电子层结构 |
下列说法中正确的是( )
| A、随原子序数的递增,第三周期元素的电负性逐渐减小 | B、氧的第一电离能比氮的第一电离能大 | C、在所有的元素中,氟的第一电离能最大 | D、在所有的元素中,氟的电负性最大 |
已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
则X、Y、Z的电负性从大到小的顺序为( )
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
| A、Z>Y>X |
| B、X>Z>Y |
| C、X>Y>Z |
| D、Y>Z>X |
在第二周期中,B、C、N、O四种元素的第一电离能由大到小的排列顺序正确的是( )
| A、I1(N)>I1(C)>I1(O)>I1(B) | B、I1(N)>I1(O)>I1(B)>I1(C) | C、I1(N)>I1(O)>I1(C)>I1(B) | D、I1(O)>I1(N)>I1(C)>I1(B) |
下列说法中正确的是( )
| A、因为P轨道是“8”字形的,所以P电子走“8”字形 | B、在第三能层中,有3s,3p,3d,3f四个轨道 | C、氢原子中只有一个电子,故氢原子只有一个轨道 | D、电子层是电子在核外空间出现概率密度分布的形象化描述 |
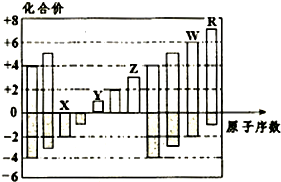 如图所示是部分短周期元素化合价与原子序数 的关系图,下列说法正确的是( )
如图所示是部分短周期元素化合价与原子序数 的关系图,下列说法正确的是( )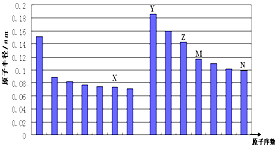 如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )
如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )