下列说法正确的是( )
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/KJ?mol-1 | 348 | 610 | 413 | 436 |
| A、已知某温度下纯水中的c (H+)=2×10-7mol?L-1,据此无法求出水中的c (OH-) |
| B、已知MgCO3的Ksp=6.82×10-6,则在含有固体MgCO3的MgCl2和Na2CO3溶液中,都有c (Mg2+)=c (CO32-),且Ksp (MgCO3)都保持不变 |
C、已知上表数据可以计算出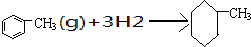 的焓变 的焓变 |
| D、常温下,Mg(OH)2能溶于氯化铵浓溶液的主要原因是NH4+结合OH-使沉淀溶解平衡发生移动 |
下列说法中不正确的是( )
| A、气体单质中,一定有σ键,可能有π键 | B、两个原子之间形成共价键时,最多有一个σ键 | C、σ键比π键重叠程度大,形成的共价键强 | D、N2分子中有一个σ键,两个π键 |
铵根离子中存在的化学键类型按离子键、共价键和配位键分类,应含有( )
| A、离子键和共价键 | B、离子键和配位键 | C、配位键和共价键 | D、离子键 |
下列说法正确的是(NA为阿伏加德罗常数)( )
| A、124gP4含有P一P键的个数为4NA | B、12g石墨中含有C-C键的个数为1.5NA | C、12g金刚石中含有C-C键的个数为4NA | D、60gSiO2中含Si一O键的个数为2NA |
关于氢键的下列说法正确的是( )
| A、没有氢键,就没有生命 | B、氢键只能存在于分子间,不能存在于分子内 | C、相同量的水在固态、液态和气态时均有氢键,且氢键的数目依次增多 | D、由于氢键的作用,使NH3,H2O,HF的沸点反常,且沸点高低顺序为:HF>H2O>NH3 |
下列变化或数据与氢键无关的是( )
| A、水凝结成冰时,密度变小 | B、氨分子与水分子形成一水合氨 | C、水在2000℃时,只有4%的H2O发生分解 | D、SbH3的沸点比PH3高 |
有四种烷烃:①3,3-二甲基戊烷、②庚烷、③2-甲基己烷、④丁烷.它们的沸点由高到低的顺序是( )
| A、②>③>①>④ | B、③>①>②>④ | C、②>③>④>① | D、②>①>③>④ |
在CH3COCH3(丙酮)分子中,羰基碳原子与甲基碳原子成键时所采取的杂化方式分别为( )
| A、sp2杂化;sp2杂化 | B、sp3杂化;sp3杂化 | C、sp2杂化;sp3杂化 | D、sp杂化;sp3杂化 |
2009年12月7日,《联合国气候变化框架公约》第15次缔约方会议在丹麦首都哥本哈根召开,192个国家和地区的代表出席了会议.此次会议被视为全人类联合遏制全球变暖行动一次很重要努力.能使气候变暖的主要气体是( )
| A、中心原子是以 SP杂化的直线型分子NO2 | B、中心原子是以 SP2杂化的∨型分子SO2 | C、中心原子是以 SP杂化的直线型分子H2S | D、中心原子是以 SP杂化的直线型分子CO2 |
下列分子的空间构型可用sp2杂化轨道来解释的是( )
①BF3②CH2=CH2 ③苯 ④乙炔 ⑤NH3⑥CH4.
①BF3②CH2=CH2 ③苯 ④乙炔 ⑤NH3⑥CH4.
| A、①②③ | B、①⑤⑥ | C、②③④ | D、③⑤⑥ |