将0.1mol/L醋酸溶液加水稀释,下列说法正确的是( )
| A、溶液中c(H+)和c(OH-)都减小 | B、水的离子积不变 | C、醋酸电离平衡向左移动 | D、溶液中c(H+)增大 |
室温下向0.1mol?L-1氨水中逐滴加入盐酸,下列叙述正确的是( )
| A、实验过程中水的电离程度是先减小后增大 | B、当滴加盐酸至溶液pH<7时,溶液中溶质一定是HCl和NH4Cl | C、当滴加盐酸至溶液pH=7时,溶液中c(NH4+)>c(Cl-) | D、当滴加盐酸至恰好完全中和时,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
已知Ag2SO4的KSP=c2(Ag+)×c(SO42-)=1.4×10-5,将适量Ag2SO4固体溶于100mL水中至刚好饱和,此时溶液中c(Ag+)=0.030mol?L-1.若t1时刻改变条件,下图中不正确的是( )
A、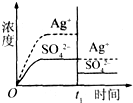 加入100mL蒸馏水 | B、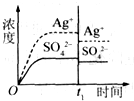 加入100mL 0.010mol?L-1 Ag2SO4 | C、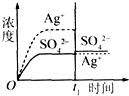 加入100mL 0.020mol?L-1 Na2SO4溶液 | D、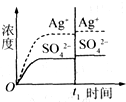 加入100mL 0.040mol?L-1 AgNO3溶液 |
下列离子方程式正确的是( )
| A、Cl2通入到NaOH溶液中:Cl2+20H-?Cl-+Cl0-+H2O | ||||
B、用惰性电极电解氯化镁溶液:2Cl-+2H20
| ||||
| C、硫化钠水溶液呈碱性的原因:S2-+2H20?H2S+20H- | ||||
| D、少量S02通入NaCl0溶液中:S02+2Cl0-+H20?SO32-+2HClO |
有关溶液中所含离子的检验,下列判断中正确的是( )
| A、加入AgNO3溶液生成的白色沉淀不溶于稀盐酸,则原溶液中一定有Cl-存在 | B、加入氨水生成白色沉淀,氨水过量时白色沉淀消失,则原溶液中一定有Al3+存在 | C、加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定有NH4+存在 | D、加入盐酸有使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量CO32-存在 |
下列有关室温时电解质溶液的叙述可能正确的是( )
| A、同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 | B、pH=a的强酸与pH=b的碱等体积混合后,溶液的pH=7 | C、稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小 | D、在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |