在通常条件下,下列各组物质的性质排列正确的是( )
| A、熔点:CO2>KCl>SiO2 | B、沸点:乙烷>正丁烷>异丁烷 | C、热稳定性:HF>NH3>H2O | D、酸性:H2SO4>H2CO3>H2SiO3 |
同一主族元素X、Y、Z三种元素,已知最高价氧化物对应的水化物的酸性强弱的酸性的顺序是:H3XO4<H3YO4<H3ZO4 下列推断正确的( )
| A、元素的非金属性X>Y>Z | B、气态氢化物稳定性XH3>YH3>ZH3 | C、最高化合价X>Y>Z | D、原子量X>Y>Z |
下列能说明氯的非金属性比溴强的事实( )
| A、共用电子对偏向:H-Cl>H-Br | B、酸性:HClO4>HBrO4 | C、熔点:Cl2<Br2 | D、酸性:HCl<HBr |
下列结论错误的是( )
| A、微粒半径:K+>Na+>Al3+>Cl- | B、氢化物的稳定性:HCl>H2S>PH3>SiH4 | C、酸性:H2SO4>H3PO4>H2CO3>HClO | D、金属性:Be<Mg<Ca<K |
下列说法正确的是( )
| A、NaOH、KOH、RbOH的碱性逐渐减弱 | B、CH4比SiH4的化学性质稳定,所以碳元素的非金属性比硅元素弱 | C、元素周期律是元素原子核外电子排布随着相对原子质量的递增发生周期性变化的必然结果 | D、砹单质为有色固体,可能易溶于某些有机溶剂,HAt不稳定,AgAt不溶于水 |
短周期主族元素X、Y、Z、W在元素周期表中的相对位置如表中所示.下列判断不正确的是( )
| Y | W | |
| X | Z |
| A、原子半径最大的是X |
| B、电负性最大的是W |
| C、Y、Z原子序数差为8 |
| D、氢化物最稳定的是Z |
X、Y为两种短周期元素,Y的原子序数比X大2.下列判断正确的是( )
| A、若X、Y同主族,则Y原子半径大于X原子半径 | B、若X、Y同周期,则X、Y只能形成离子化合物 | C、若X为碳元素,则Y的气态氢化物的分子为非极性分子 | D、若X为铝元素,则Y最高价氧化物对应的水化物为强酸 |
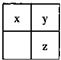 短周期主族元素x、y、z在元素周期表中的相对位置如图,下列推论合理的是( )
短周期主族元素x、y、z在元素周期表中的相对位置如图,下列推论合理的是( )| A、若y和z能形成化合物,则x为氮元素 | B、若x、y、z的单质常温下都是气体,则Y为氧元素 | C、若x、y、z是非金属元素,则它们气态氢化物的水溶液都显酸性 | D、若x、y、z的原子序数之和小于20,则它们都是金属元素 |
下列说法正确的是( )
| A、S、P、Cl得电子能力和它们相应的最高价氧化物对应水化物的酸性均依次增强 | B、工业上通常用电解Na、Mg、Al对应的氯化物制得该三种金属单质 | C、金属钠着火时,用干细沙覆盖灭火 | D、淀粉、纤维素和油脂都属于天然高分子化合物 |
下列有关元素周期律的叙述正确的是( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4 ④离子半径:Cl->S2->K+
⑤碱性:Ca(OH)2>Mg(OH)2>Al(OH)3.
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4 ④离子半径:Cl->S2->K+
⑤碱性:Ca(OH)2>Mg(OH)2>Al(OH)3.
| A、①③ | B、②⑤ | C、②④ | D、③⑤ |