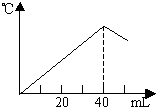
 运用中和热的测定方法,在绝对保温、隔热的条件下,向20mL2.08mol/L的NaOH溶液中逐滴加入未知浓度的H2SO4(边加边充分搅拌)后,测得溶液的温度与滴加H2SO4溶液体积关系如图所示,则该H2SO4溶液的物质的量浓度约是( )
运用中和热的测定方法,在绝对保温、隔热的条件下,向20mL2.08mol/L的NaOH溶液中逐滴加入未知浓度的H2SO4(边加边充分搅拌)后,测得溶液的温度与滴加H2SO4溶液体积关系如图所示,则该H2SO4溶液的物质的量浓度约是( )| A、2.08mol/L | B、1.04mol/L | C、4.16mol/L | D、0.52mol/L |
奥运会火炬可用丙烷或丁烷作燃料.已知丙烷的沸点为-42.1℃,燃烧热为2219.2kJ/mol;正丁烷的沸点为-0.5℃,燃烧热为2877.6kJ/mol.下列判断中错误的是( )
| A、奥运火炬中燃料燃烧主要是将化学能转变为热能和光能 | B、烷烃沸点和燃烧热都随碳原子数增加而成比例递增 | C、异丁烷的沸点肯定低于-0.5℃ | D、正己烷在常温常压下肯定不是气体 |
“摇摇冰”是一种即用即冷的饮料,吸食时将饮料罐隔离层中的化学物质和水混合摇动即会制冷.其化学原理是( )
| A、生石灰与水反应放出大量的热 | B、硝酸铵溶于水能吸热 | C、硝酸铵溶于水呈酸性 | D、生石灰溶于水呈碱性 |
下列叙述正确的是( )
| A、在钢铁中加入任何金属元素,都会使钢铁的抗腐蚀能力减小 | B、用铝质铆钉接铁板,铁易被腐蚀 | C、马口铁(镀锡)的表面一旦破损,铁腐蚀加快 | D、纯铁比生铁抗腐蚀 |
认真观察各实验的示意图,其中正确的是( )
A、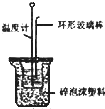 测定中和热 | B、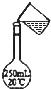 配制100mL0.10mol/L盐酸 | C、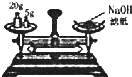 称量氢氧化钠固体 | D、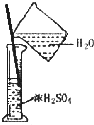 浓硫酸的稀释 |
目前科学家已经开发出便携式固体氧化物燃料电池,它以烷烃气体为燃料,每填充一次燃料,可连续几小时,甚至几十小时以50W的功率向外输出电能.这种电池的一极通入的是空气,而另一极通入的是烷烃气体;电解质是一种固体氧化物,该固体氧化物在熔融状态下能传导O2-.下列对该燃料电池说法中正确的是( )
| A、在熔融电解质中,O2-由负极移向正极 | B、通甲烷的电极为电池的正极 | C、负极的电极反应方程式为:CH4+4O2--8e-?CO2+2H2O | D、电路中每流过1mol电子,约有5.6L甲烷被完全氧化 |
电动自行车由于灵活、快捷、方便,已成为上班族的主要代步工具,其电源常用铅蓄电池,反应原理为:PbO2+Pb+2H2SO4
2PbSO4+2H2O 下列叙述正确的是( )
| 放电 |
| 充电 |
| A、放电时PbO2是电池的负极,电解质溶液的密度逐渐减小 |
| B、放电时负极的电极反应式为:Pb+SO42--2e-?PbSO4↓ |
| C、电池充电时,PbO2得电子被氧化 |
| D、电池充电时,阴极电极反应式为:PbSO4+2H2O-2e-?PbO2+SO42-+4H+ |
已知下列两个气态物质之间的反应:C2H2(g)+H2(g)?C2H4(g)…①,
2CH4(g)?C2H4(g)+2H2(g)…②.
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)?CH4(g),△H=-Q1…Ⅰ
C(s)+
H2(g)?
C2H2(g),△H=-Q2…Ⅱ
C(s)+H2(g)?
C2H4(g),△H=-Q3…Ⅲ(Q1、Q2、Q3均为正值),
“Q值”大小比较正确的是( )
2CH4(g)?C2H4(g)+2H2(g)…②.
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)?CH4(g),△H=-Q1…Ⅰ
C(s)+
| 1 |
| 2 |
| 1 |
| 2 |
C(s)+H2(g)?
| 1 |
| 2 |
“Q值”大小比较正确的是( )
| A、Q1>Q3>Q2 |
| B、Q1>Q2>Q3 |
| C、Q2>Q1>Q3 |
| D、Q3>Q1>Q2 |
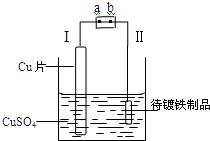 右图是在待镀铁制品上镀铜的实验装置,则下列说法正确的是( )
右图是在待镀铁制品上镀铜的实验装置,则下列说法正确的是( )