下列对教材中的数据叙述正确的是( )
| A、单独利用焓变的数据或熵变的数据就能判断化学反应能否自发进行 | B、利用沸点数据可以推测将一些液体混合物分离开来的可能性 | C、利用反应热数据的大小可以判断不同反应的反应速率的大小 | D、利用溶液的pH与7的大小关系,可以判断任何温度下溶液的酸碱性 |
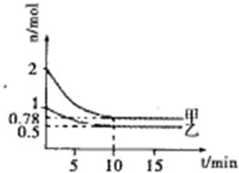 向甲、乙两容积均为1L的恒容容器中分别充入2molPCl3、2molCl2和1molPCl3、1molCl2,T℃时,发生如下反应PCl3(g)+Cl(g)?PCl5(g)△H<0测得窗口中n(PCl3)随时间t的变化如图所示,下列叙述错误的是( )
向甲、乙两容积均为1L的恒容容器中分别充入2molPCl3、2molCl2和1molPCl3、1molCl2,T℃时,发生如下反应PCl3(g)+Cl(g)?PCl5(g)△H<0测得窗口中n(PCl3)随时间t的变化如图所示,下列叙述错误的是( )| A、在0-10min内甲容器中PCl3的反应速率为v(PCl3)=0.122mol?L-1?min-1 | B、在T℃时,该反应的平衡常数K甲=K乙 | C、若向平衡后的乙容器中充入PCl3(g),则再次达到平衡时PCl3的体积分数增大 | D、升高甲容器的温度,可以使甲容器中各物质的体积分数与乙容器的相同 |
在三个2L恒容的容器中,分别发生反应A(g)+3B(g)?2C(g) 5min后各容器反应达平衡状态,其中甲容器中A的物质的量为0.4mol.
下列说法正确的是( )
| 反应前各物质的物质的量/mol | |||
| A | B | C | |
| 甲 | 1 | 3 | 0 |
| 乙 | 0 | 0 | 2 |
| 丙 | 1.5 | 4.5 | 1 |
| A、乙中5min内C的反应速率为0.12mol/(L?min) |
| B、达到平衡时,甲乙两容器中C的物质的量百分含量相等 |
| C、达到平衡时,丙中A的浓度是甲中的2倍 |
| D、丙中反应的平衡常数大于甲中反应的平衡常数 |
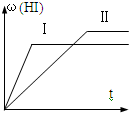 将1molH2(g)和2molI2(g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+I2(g)?2HI(g)△H<0,并达到平衡,HI的体积分数ω(HI)随时间变化如图(Ⅱ)所示.若改变反应条件,ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是( )
将1molH2(g)和2molI2(g)置于某2L密闭容器中,在一定温度下发生反应:H2(g)+I2(g)?2HI(g)△H<0,并达到平衡,HI的体积分数ω(HI)随时间变化如图(Ⅱ)所示.若改变反应条件,ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是( )| A、恒温恒容条件下,加入适当催化剂 | B、恒温条件下,缩小反应容器体积 | C、恒容条件下升高温度 | D、恒温条件下,扩大反应容器体积 |
在N2+3H2
2NH3的反应中,在5s中N2由6mol/L减至2mol/L.则NH3的平均反应速率是( )
| ||
| 高温高压 |
| A、2.4 mol/(L?s) |
| B、1.6mol/(L?s) |
| C、0.8 mol/(L?s) |
| D、0.08 mol/(L?s) |
一定条件下,将3molA和1molB两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g)+2D(s).2min末该反应达到平衡,生成0.8molD,并测得C的浓度为0.2mol/L.下列判断正确的是( )
| A、该条件下此反应的化学平衡常数约为0.91(L/mol)3 | B、A的平均反应速率为0.3mol/(L?s) | C、B的转化率为60% | D、若混合气体的密度不再改变时,该反应不一定达到平衡状态 |
在一定条件下,某密闭容器中发生了如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0平衡后,SO2、O2、SO3的物质的量之比为3:2:5.保持其它条件不变,升温后达到新平衡时,SO2、O2的物质的量分别为1.4mol和0.9mol,此时容器内SO3的物质的量应为( )
| A、1.8mol | B、2mol | C、2.2 mol | D、2.4mol |
在体积、温度都相同的条件下有下列反应:2A(g)+2B(g)?C(g)+3D(g).现分别从两条途径建立平衡:
I.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下叙述中不正确的是( )
I.A、B的起始物质的量均为2mol,
Ⅱ.C、D的起始物质的量分别为2mol和6mol.
以下叙述中不正确的是( )
| A、I、Ⅱ两途径最终达到平衡时,体系内混合气的百分组成相同 | ||
| B、I、Ⅱ两途径最终达到平衡时,体系内混合气的平均相对分子质量相同 | ||
| C、达平衡时,I途径的反应速率vA等于Ⅱ途径的反应速率vA | ||
D、达平衡时,I途径所得混合气的密度为Ⅱ途径所得混合气密度的
|
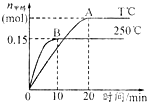 将1mol CO和2mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生 反应:CO(g)+2H2(g)═CH3OH(g),△H=a kJ/mol,如图.下列分析中正确的是( )
将1mol CO和2mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生 反应:CO(g)+2H2(g)═CH3OH(g),△H=a kJ/mol,如图.下列分析中正确的是( )| A、250℃时,0-10minH2 反应速率为 0.015 mol/(L?min) | B、平衡时CO的转化率:T℃时小于250℃时 | C、其他条件不变,若减小容积体积,CO体积分数增大 | D、a<0,平衡常数K:T℃时大于250℃ |
 4NO(g)+6H2O(g)+3623KJ;下列叙述正确的是( )
4NO(g)+6H2O(g)+3623KJ;下列叙述正确的是( )