根据所学的知识和经验,判断下列变化在常温下的焓变、熵变及方向性,填表:
(说明:△H、△S填“>0”、“<0”、“=”,方向性填“可以自发”、“不能自发”或“无法确定”)
| 变化 | △H | △S | 方向性 |
| NH4Cl(s)═NH3(g)+HCl(g) | |||
| 2H+(aq)+Zn(s)═Zn2+(aq)+H2(g) |
密闭容器中X、Y、Z三种气体的初始浓度和不同温度下的平衡浓度如下表:
|
PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生反应,在10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g).有关数据如下:
下列判断错误的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol/L) | c1 | c2 | 0.4 |
| A、10 min内,v(Cl2)=0.04 mol/(L?min) |
| B、当反应达到平衡时,容器中Cl2为1.2 mol |
| C、若升高温度反应的平衡常数减小,则平衡时PCl3的转化率变大 |
| D、平衡后再加入2.0 mol PCl3,在相同条件下再达平衡时,c(PCl5)<1.0mol/L |
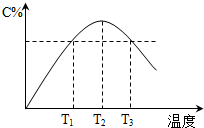 在某体积固定的密闭容器中进行如下可逆反应:A(g)+B(g)?2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示.下列说法正确的是( )
在某体积固定的密闭容器中进行如下可逆反应:A(g)+B(g)?2C(g),在反应过程中体系的温度持续升高,实验测得混合气体中C的含量与温度关系如图所示.下列说法正确的是( )| A、此反应的正反应是吸热反应 | B、反应在T2温度时达到平衡 | C、T3温度时正反应速率大于逆反应速率 | D、T3温度时正反应速率大于T1温度时正反应速率 |
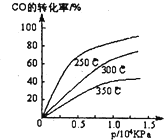 工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH30H(g)
工业上一般在密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)?CH30H(g)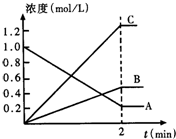 如图表示800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t表示时间.试回答:
如图表示800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t表示时间.试回答: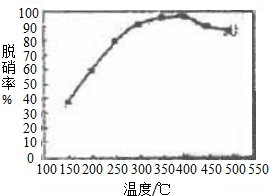 NOX是生成光化学烟雾、破坏臭氧层和形成酸雨的前驱气体之一.烟道气中氮氧化物可采用氨气催化脱硝,右图是相同流速不同温度下的脱硝率,反应方程式可表示为2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g),下列说法正确的是( )
NOX是生成光化学烟雾、破坏臭氧层和形成酸雨的前驱气体之一.烟道气中氮氧化物可采用氨气催化脱硝,右图是相同流速不同温度下的脱硝率,反应方程式可表示为2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g),下列说法正确的是( )