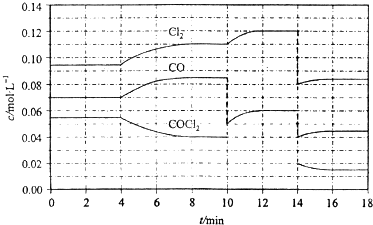
光气(COCl2)的分解反应为:COCl2(g)?Cl2(g)+CO(g)△H=+108kJ?mol-1.反应体系中各物质的浓度在不同条件下的变化如图8所示(10~14min的COCl2浓度变化未标出):
下列说法正确的是( )

下列说法正确的是( )
| A、COCl2在5~6 min和15~16 min时平均反应速率:v(5~6)>v(15~16) | B、第10 min时,改变反应条件,反应重新达到平衡前:v(正)<v(逆) | C、第12 min时,反应重新达到平衡,c(COCl2)≈0.03 mol?L-1 | D、第14 min时,改变的条件是减小压强,随着平衡的移动,COCl2的转化率减小 |
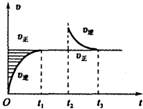 某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?),在t1时刻反应达到平衡,在t2时刻缩小容器体积,至t3时刻再次达到平衡,反应速率与时间的关系如图.下列有关叙述正确的是( )
某恒温密闭容器发生可逆反应Z(?)+W(?)?X(g)+Y(?),在t1时刻反应达到平衡,在t2时刻缩小容器体积,至t3时刻再次达到平衡,反应速率与时间的关系如图.下列有关叙述正确的是( )| A、Z、W一定不为气体,Y可能为气体,也可能不为气体 | B、t2时刻后该可逆反应向逆反应方向进行,Y的浓度一定减小 | C、在t2时刻加入催化剂,反应速率变化情形与图中t2时刻后类似 | D、若该反应的△H<0,在t2时刻升温,反应速率变化情形与图中t2时刻后类似 |
在1L密闭容器中发生反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-Q kJ?mol-1(Q>O),容器内部分物质的物质的量浓度如下表:
|
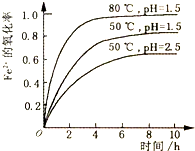 酸性溶液中,Fe2+会被空气缓慢氧化为Fe3+.不同条件下,一定浓度的Fe2+的氧化率随时间变化关系如图所示.下列有关说法正确的是( )
酸性溶液中,Fe2+会被空气缓慢氧化为Fe3+.不同条件下,一定浓度的Fe2+的氧化率随时间变化关系如图所示.下列有关说法正确的是( )| A、该氧化过程的离子方程式为:Fe2++O2+4H+=Fe3++2H2O | B、pH=1.5时Fe2+的氧化率一定比pH=2.5的大 | C、Fe2+的氧化率仅与溶液的pH和温度有关 | D、其他条件相同时,80℃时Fe2+的氧化率比50℃的大 |
 在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:
在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3X(g)+Y(g)?2Z(g)△H<0
保持温度不变,测得平衡时的有关数据如下:
| 恒容容器甲 | 恒压容器乙 | |
| Y的物质的量(mol) | n1 | n2 |
| Z的体积分数 | φ1 | φ2 |
| A、平衡时容器乙的容积一定比反应前小 |
| B、φ2>φ1 |
| C、n2>n1 |
| D、平衡时容器甲的压强一定比反应前大 |
下列哪个是影响化学反应速率的主要因素( )
| A、压强 | B、温度 | C、催化剂 | D、反应物的性质 |
在一定条件下,已达平衡的可逆反应:2A(g)+B(g)?2C(g),下列说法中正确的是( )
A、平衡时,此反应的平衡常数K与各物质的浓度有如下关系:K=
| ||
| B、改变条件后,该反应的平衡常数K一定不变 | ||
| C、如果改变压强并加入催化剂,平衡常数会随之变化 | ||
| D、若平衡时增加A和B的浓度,则平衡常数会减小 |
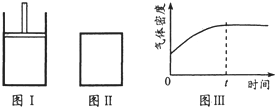 如图所示,图I是恒压密闭容器,图II是恒容密闭容器.当其它条件相同时,在I、II中分别加入2mol X和2mol Y,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)?aZ(g),此时I中X、Y、Z的物质的量之比为1:3:2.下列判断正确的是( )
如图所示,图I是恒压密闭容器,图II是恒容密闭容器.当其它条件相同时,在I、II中分别加入2mol X和2mol Y,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)?aZ(g),此时I中X、Y、Z的物质的量之比为1:3:2.下列判断正确的是( )