现将X、Y、Z、W四种纯金属两两组合,用导线连接后分别插入到浓度相同的稀H2SO4或CuSO4溶液中形成原电池,结果如下:X、Y组合时,X为负极;Z、W组合时,W上发生氧化反应;Y、Z组合时,Y变细,Z变粗;Y、W组合时,W上有气泡产生.则X、Y、Z、W四种金属的活泼性由强到弱的顺序正确的是( )
| A、X>Y>Z>W | B、X>Y>W>Z | C、W>Z>X>Y | D、X>Z>Y>W |
生产铅蓄电池时,在两极板的铅锑合金上均匀涂上膏状的PbSO4,干燥后安装,充电后即可使用,发生的反应为:2PbSO4+2H2O
Pb+PbO2+2H2SO4.下列说法错误的是( )
| 充电 |
| 放电 |
| A、该电池需要定期补充H2SO4 |
| B、电池工作时,铅是负极,PbO2是正极 |
| C、电池工作时,电解质溶液的密度减小 |
| D、电池充电时,溶液的pH减小 |
下列各项正确的是( )
| A、O2+2H2O+4e-?4OH-碱性环境下氢氧燃料电池的负极反应 | B、4OH--4e-?O2↑+2H2O弱酸性环境下钢铁的吸氧腐蚀 | C、2H++2e-?H2↑用Cu作电极电解NaOH溶液的阴极反应 | D、H2-2e-?2H+用惰性电极电解H2SO4的阳极反应 |
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,越来越成为人们研制绿色原电池的关注焦点.其中一种镁原电池的反应为:xMg+Mo3S4
MgMo3S4,下列说法正确的是( )
| 放电 |
| 充电 |
| A、电池放电时,Mg2+向负极迁移 |
| B、电池放电时,正极反应为Mo3S4+2xe-+xMg2+?MgxMo3S4 |
| C、电池充电时,阴极发生还原反应生成Mo3S4 |
| D、电池充电时,阳极反应为xMg-2xe-?xMg2+ |
 如图为原电池示意图,下列说法中正确的是( )
如图为原电池示意图,下列说法中正确的是( )| A、锌片是负极 | B、铜片是负极 | C、电子由铜片通过导线流向锌片 | D、该装置能够将电能转化为化学能 |
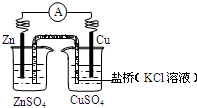 铜锌原电池(如图)工作时,下列叙述正确的是( )
铜锌原电池(如图)工作时,下列叙述正确的是( )| A、外电路中,电子从锌棒经导线流向铜棒 | B、电池总反应为:Zn+2H+?Zn2++H2↑ | C、正极反应为:Zn-2e-?Zn2+ | D、盐桥中的K+移向ZnSO4溶液 |
在理论上不能用于设计原电池的化学反应为( )
| A、Mg3N2+6H2O?3Mg(OH)2+2NH3 | B、2H2(g)+O2(g)?2H2O(l)△H<0 | C、2Zn(s)+O2(g)?2ZnO(s) | D、4Fe(OH)2+O2+2H2O?4Fe(OH)3 |
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示:
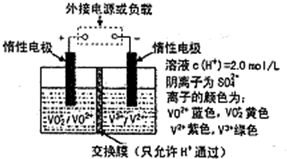
下列说法错误的是( )

下列说法错误的是( )
A、当左槽溶液逐渐由黄变蓝,其电极反应式为VO
| ||
| B、充电时若转移的电子数为3.01×1023,则左槽溶液中行n(H+)最终的变化量为1mol | ||
| C、放电过程中,氢离子的作用之一是参与正极反应 | ||
| D、充电过程中,右槽溶液颜色逐渐由绿色变为紫色 |
 铜锌原电池(如图)工作时,下列叙述正确的是( )
铜锌原电池(如图)工作时,下列叙述正确的是( )