已知:H2O(l)═HO(g)△H=Q1 kJ/mol
H2O(g)═2H2(g)+O2(g)△H=Q2 kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-Q3kJ/mol
则H2和CH4的燃烧热之比是( )
H2O(g)═2H2(g)+O2(g)△H=Q2 kJ/mol
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-Q3kJ/mol
则H2和CH4的燃烧热之比是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
由金红石(TiO2)制备单质Ti,涉及的步骤为TiO2→+TiCl4
Ti.已知:①C(s)+O2(g)═CO2(g)△H=-393.5kJ?mol??,②2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol??,③TiO2(s)+2a2(g)═TiCl4(s)+O2(g)△H=+14l kJ?mol??.下列叙述正确的是( )
| Mg |
| 800℃,Ar |
| A、CO的燃烧热为566 kJ?mol?? |
| B、反应③为放热反应 |
| C、1 mol C(s)燃烧生成1 mol CO(g)放出的热量为172.5 kJ |
| D、TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的反应热为-80 kJ?mol?? |
根据表中的信息判断下列说法正确的是( )
| 物质 | 金刚石 | 石墨 |
| 外观 | 无色,透明固体 | 灰黑,不透明固体 |
| 熔点 | ? | ? |
| 燃烧热/KJ?mol-1 | 395.4 | 393.5 |
A、表示石墨燃烧热的热化学方程式为C(石墨,s)+
| ||
| B、由表中信息知C(石墨,s)═C(金刚石,s)△H=+1.9 kJ?mol?? | ||
C、由表中信息可得如图所示的图象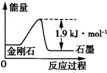 | ||
| D、由表中信息可推知相同条件下金刚石的熔点高于石墨的 |
生产液晶显示器过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12000~20000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
下列说法中正确的是( )
| 化学键 | N≡N | F-F | N-F |
| 键能/KJ?mol-1 | 941.7 | 154.8 | 283.0 |
| A、过程N2(g)→2N(g)放出能量 |
| B、过程N(g)+3F(g)→NF3(g)放出能量 |
| C、反应N2(g)+3F2(g)→2NF3(g)的△H>0 |
| D、NF3吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应 |
 我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列有关说法正确的是( )
我国新建的某海岛发电示意图如图,已知铅蓄电池放电时的总反应为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,下列有关说法正确的是( )| A、图中涉及的能量转化方式只有3种 | ||
B、蓄电池供电时,负极的电极反应为:Pb+SO
| ||
| C、储能时若充电时间过长,阳极流向阴极的气体可能是H2 | ||
| D、该发电工艺不可实现零排放 |
下列有关说法正确的是( )
| A、反应2Mg(s)+CO2(g)=C(s)+2MgO(s)能自发进行,则该反应的△H>0 | ||
| B、水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 | ||
C、常温下,将醋酸稀溶液加水稀释,溶液中
| ||
| D、饱和碳酸钠溶液可将BaSO4粉末转化为BaCO3,说明Ksp(BaSO4)>Ksp(BaCO3) |
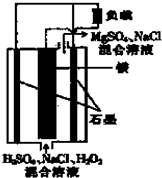 镁-过氧化氢燃料电池具有能量高、安全方便等优点,其总反应为Mg+H2O2+H2SO4?MgSO4+2H2O.结构示意图如图所示.下列关于该电池的叙述正确的是( )
镁-过氧化氢燃料电池具有能量高、安全方便等优点,其总反应为Mg+H2O2+H2SO4?MgSO4+2H2O.结构示意图如图所示.下列关于该电池的叙述正确的是( )| A、电池内部可以使用MnO2作填料 | B、电流工作时,H+向Mg电极移动 | C、电池工作时,正极的电极反应式为Mg-2e-?Mg2+ | D、电池工作时,电解质溶液的pH将不断变大 |
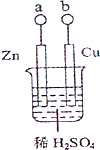 某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )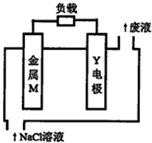 锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中,电池的基本结构如图所示.下列说法正确的是( )
锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中,电池的基本结构如图所示.下列说法正确的是( )