0 21334 21342 21348 21352 21358 21360 21364 21370 21372 21378 21384 21388 21390 21394 21400 21402 21408 21412 21414 21418 21420 21424 21426 21428 21429 21430 21432 21433 21434 21436 21438 21442 21444 21448 21450 21454 21460 21462 21468 21472 21474 21478 21484 21490 21492 21498 21502 21504 21510 21514 21520 21528 203614
 化学反应A2+B2═2AB的能量变化如图所示,则下列说法正确的是( )
化学反应A2+B2═2AB的能量变化如图所示,则下列说法正确的是( )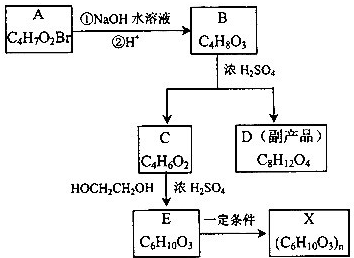
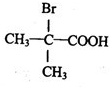
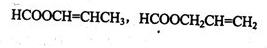
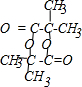
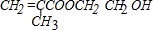
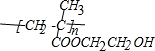
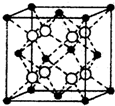 (2013?烟台一模)【化学--物质结构与性质】
(2013?烟台一模)【化学--物质结构与性质】

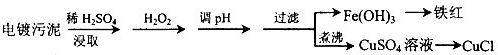
 (2013?烟台一模)氮及其化合物在工农业生产中具有重要作用.
(2013?烟台一模)氮及其化合物在工农业生产中具有重要作用.