0 21300 21308 21314 21318 21324 21326 21330 21336 21338 21344 21350 21354 21356 21360 21366 21368 21374 21378 21380 21384 21386 21390 21392 21394 21395 21396 21398 21399 21400 21402 21404 21408 21410 21414 21416 21420 21426 21428 21434 21438 21440 21444 21450 21456 21458 21464 21468 21470 21476 21480 21486 21494 203614
 ,下列有关它的推测,不正确的是( )
,下列有关它的推测,不正确的是( )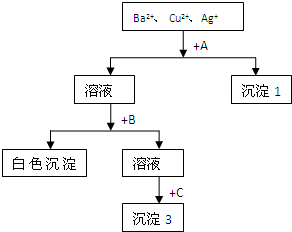 某溶液含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如右(写出最佳答案):
某溶液含有Ba2+、Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程图如右(写出最佳答案):